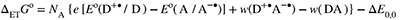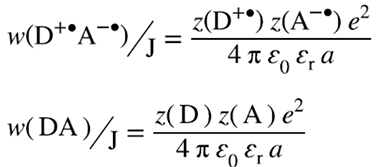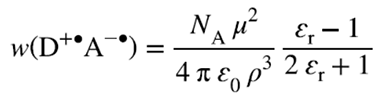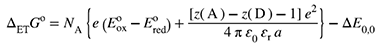ქიმიის ტერმინთა განმარტებითი ლექსიკონი
- ინგლისურ-ქართული
- ქართულ-ინგლისური
- ლექსიკონის შესახებ
- გამოხმაურება

| Gibbs energy of photoinduced electron transfer | ელექტრონის ფოტოინდუცირებული გადატანის გიბსის ენერგია |
| For photoinduced electron transfer between an acceptor (A) and a donor (D) (either one of them may be the electronically excited molecular entity) of any charge type, ȥ(A) and ȥ(B), the change in standard Gibbs energy can be approximated as (the notation is for the case of neutral species D and A)
where e = 1.602 176 487 × 10-19 C is the elementary charge, NA = 6.022 141 79 × 1023 mol-1 is the Avogadro constant, E°(D+∙/D)/V is the standard electrode potential of the donor cation radical resulting from the electron transfer, E°(A/A-∙)/V is the standard electrode potential of the acceptor (both relative to the same reference electrode) and ΔE0.0/(J mol-1) is the vibrational zero electronic energy of the excited partner (provided that a vibrationally equilibrated excited state at energy ΔE0.0 takes part in the reaction), all data referring to the same solvent. w(D+∙A-∙) and w(DA) are the electrostatic work terms that account for the effect of Coulombic attraction in the products and reactants, respectively
Where a is the distance of the charged species after electron transfer, εr is the relative medium static permittivity (formerly called dielectric constant), &epslion;r ≈ 8.854 × 10-12 C2 J-1 m-1 is the electric constant (vacuum permittivity), and ȥ(X) the charge of the species X. In SI units the factor e2/(4 π ε0) = 2.307 × 10-28 J m. For the case of neutral species A and D, ȥ(D) = ȥ(A) = 0. Notes:
with E°ox the standard electrode potential at which the oxidation occurs, and E°red the standard electrode potential at which the reduction occurs. This form of the first term within the brackets is misleading and not recommended.
|
ელექტრონის ფოტოინდუცირებული გადატანისათვის აქცეპტორსა (A) და დონორს (D) შორის (თითოეული მათგანი შეიძლება იყოს ელექტრონულად აღგზნებული მოლეკულური ერთეული) ნებისმიერი ტიპის მუხტის, ȥ(A) და ȥ(B), სტანდარტული გიბსის ენერგიის ცვლილება შეიძლება დაახლოებით ასე გამოისახოს (როდესაც D და A ნეიტრალური ნაწილაკებია)
სადაც e = 1.602 176 487 × 10-19 კულ არის ელემენტარული მუხტი, NA = 6.022 141 79 × 1023 მოლი-1 არის ავოგადროს მუდმივა, E°(D+•/D)/V არის დონორი კატიონ რადიკალის სტანდარტული ელექტროდული პოტენციალი. რადიკალი, რომელიც წარმოიქმნება ელექტრონის გადატანის შედეგად, E°(A/A-•)/V არის აქცეპტორის სტანდარტული ელექტროდული პოტენციალი (ორივე ერთსა და იმავე შესადარებელ ელექტროდთან მიმართებაში) და ΔE0.0/(ჯ მოლი-1) არის აღგზნებული პარტნიორის რხევითი ნულოვანი ელექტრონული ენერგია (იმ პირობით, რომ რეაქციაში მონაწილეობს რხევით გაწონასწორებული აღგზნებული მდგომარეობა, ΔE0.0 ენერგიით), ყველა მონაცემი ეხება ერთსა და იმავე გამხსნელს. w(D+∙A-∙) და w(DA) არის ელექტროსტატიკური მუშობის წევრები, რომლებიც ხსნიან კულონური მიზიდულობის ეფექტს, შესაბამისად, პროდუქტებსა და რეაგენტებში.
სადაც a არის მანძილი დამუხტული ნაწილაკებამდე მანძილი ელექტრონის გადატანის შემდეგ, εr არის გარემოს ფარდობითი სტატიკური დიელექტრიკული შეღწევადობა (რომელსაც ადრე დიელექტრიკული მუდმივა ეწოდებოდა), εr ≈ 8.854 × 10-12 კულ2 ჯ-1 მ-1 არის ელექტრული მუდმივა (ვაკუუმის დიელექტრიკული შეღწევადობა) , ხოლო ȥ(X) არის X ნაწილაკის მუხტი. SI ერთეულებში კოეფიციენტია e2/(4 π ε0) = 2.307 × 10-28 ჯ მ. ნეიტრალური A და D ნაწილაკების შემთხვევაში, ȥ(D) = ȥ(A) = 0. შენიშვნები:
სადაც E°ox-ით აღნიშნულია სტანდარტული ელექტროდული პოტენციალი, რომლის დროსაც ხდება ჟანგვა, ხოლო E°red აღნიშნავს სტანდარტულ ელექტროდულ პოტენციალს, რომლის დროსაც ხდება აღდგენა. პირველი ტერმინის ეს ფორმა ფრჩხილებში შეცდომაში შემყვანია და არ არის რეკომენდებული.
|
| Source | წყარო: PAC, 2007, 79, 293 (Glossary of terms used in photochemistry, 3rd edition (IUPAC Recommendations 2006)) on page 348 |
|



ჩვენი სტუმრები
სწრაფი ბმულები