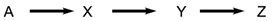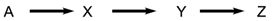A reaction that involves more than one elementary reaction is said to occur by a composite mechanism. The terms complex mechanism, indirect mechanism, and step-wise mechanism are also commonly used. There are two main kinds of evidence for a composite mechanism:
- The kinetic equation for the reaction does not correspond to its stoichiometry.
- There is experimental evidence, direct or indirect, for intermediates of such a nature that it is necessary to conclude that more than one elementary reaction is involved. There are many types of composite mechanisms, for example:
- Reactions occurring in parallel, such as:
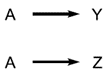
are called parallel reactions or simultaneous reactions. When there are simultaneous reactions there is sometimes competition, as in the scheme:
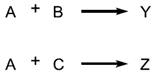
where B and C compete with one another for A.
- Reactions occurring in forward and reverse directions are called opposing reactions:

- Reactions occurring in sequence, such as
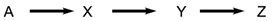
are known as consecutive reactions.
- Reactions are said to exhibit feedback if a substance formed in one step affects the rate of a previous step. For example, in the scheme:
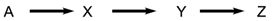
The intermediate Y may catalyse the reaction A → X (positive feedback) or it may inhibit it (negative feedback).
- Chain reactions.
|
რეაქციას, რომელიც ერთზე მეტ ელემენტარულ რეაქციას მოიცავს, რთული მექანიზმით მიმდინარეს უწოდებენ. ასევე ხშირად გამოიყენება ტერმინები კომპლექსური მექანიზმი, არაპირდაპირი მექანიზმი და ეტაპობრივი მექანიზმი. რთული მექანიზმის ორი ძირითადი ნიშანი არსებობს:
- რეაქციის კინეტიკური განტოლება არ შეესაბამება მის სტექიომეტრიას.
- ზოგიერთი ინტერმედიატის ბუნებიდან გამომდინარე, არსებობს პირდაპირი ან არაპირდაპირი ექსპერიმენტული მტკიცებულება, რომ პროცესში ჩართულია ერთზე მეტი ელემენტარული რეაქცია. არსებობს მრავალი სახის რთული მექანიზმი, მაგალითად:
- რეაქციები, რომლებიც პარალელურად მიმდინარეობს:

მათ პარალელური ან ერთდროული რეაქციები ეწოდება. ერთდროული რეაქციები ზოგჯერ კონკურენტულია, მაგალითად, მოცემულ რეაქციებში:

B და C ერთმანეთის კონკურენტებია A-სთან რეაქციაში შესასვლელად.
- პირდაპირ და საპირისპირო მიმართულებით მიმდინარე რეაქციებს საპირისპირო რეაქციები ეწოდება:

- თანამიმდევრობით მიმდინარე რეაქციები, როგორიცაა:
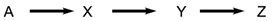
ცნობილია, როგორც თანამიმდევრული რეაქციები.
- რეაქციებს ეწოდება უკუკავშირის გამომხატველი, თუ ერთ საფეხურზე წარმოქმნილი ნივთიერება გავლენას ახდენს წინა საფეხურის სიჩქარეზე. მაგალითად, სქემაში:
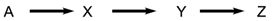
შუალედურმა Y ნივთიერებამ შეიძლება მოახდინოს A → X რეაქციის კატალიზება (დადებითი უკუკავშირი) ან ინჰიბირება (უარყოფითი უკუკავშირი).
- ჯაჭვური რეაქციები.
|