6.მე-6 ჯგუფის ელემენტები
6.1.ქრომი
კითხვა:
რომელ ლიგანდებთან წარმოქმნის კომპლექსნაერთებს ქრომი ნულოვანი ჟანგვითი რიცხვით?
პასუხი:
კარბონილურ კომპლექსებში ქრომის (მისი ანალოგების) ატომები ნულოვანი ჟანგვითი რიცხვით შეიძლება დავახასიათოთ d6 ელექტრონული კონფიგურაციით:
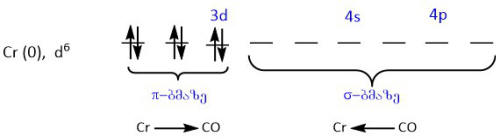
CO-ს მოლეკულის ელექტრონული კონფიგურაციაა:

ელექტრონებით დაკავებული ორი არამაკავშირებელი σ°-ორბიტალი შეესაბამება ელექტრონების ორ არამაკავშირებელ წყვილს, რომელთაგან ერთი ეკუთვნის ჟანგბადის ატომს, ხოლო მეორე - ნახშირბადის ატომს. დონორულ-აქცეპტორულ ურთიერთქმედებაში მონაწილეობისათვის ელექტრონული წყვილი ენერგეტიკულად უფრო ხელსაყრელია, ვიდრე -ელექტრონული წყვილი. ამიტომ ლიგანდის სახით CO-ს მოლეკულა უპირატესად კოორდინირდება ნახშირბადის ატომის მეშვეობით. ქრომის Cr(0) ატომის ექვსი თავისუფალი 3d24s14p3 ორბიტალისა და C-ს ატომით CO-ს ექვსი მოლეკულის არამაკავშირებელი ელექტრონული წყვილის ხარჯზე წარმოიქმნება ექვსი σ-ბმა Cr ← CO და Cr(СО)6-ის მოლეკულა.
ქრომის ჰექსაკარბონილის მოლეკულის - Cr(СО)6-ის სტაბილიზაცია მიიღწევა p-დატიური ურთიერთქმედების (Cr→CO) ხარჯზე, რომელშიც მონაწილეობენ ქრომის ატომის 3d-ელექტრონული წყვილები და CO-ს მოლეკულის თავისუფალი π*-ორბიტალები. CO-დან Cr-ის ატომისკენ (s-დონორულ-აქცეპტორული ურთიერთქმედებისას) და Cr-ის ატომიდან CO-ს მოლეკულისკენ (p-დატიური ურთიერთქმედებისას) მუხტის გადატანის შედეგად ჯამური მუხტი ქრომის ატომზე დადებითი ხდება δCr = 0.4.
მუხტის გადატანა s-ბმის (M←CO) და p-ბმის (M→CO) წარმოქმნისას იწვევს ბმის რიგის შემცირებას CO-ს მოლეკულაში. მაგალითად, ინფრაწითელი სპექტრების მიხედვით, CO-ს თავისუფალი მოლეკულისათვის nCO = 2155 სმ-1-ს, ხოლო კოორდინირებული CO-ჯგუფებისათვის - უფრო ნაკლებია, დაახლოებით 2000 სმ-1.
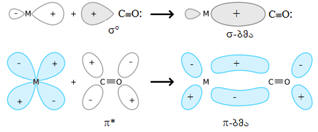
M → CO σ- და π-ბმების წარმოქმნა d-ელემენტების კარბონილებში:
ფერადი ორბიტალები დასახლებული ორბიტალებია; თეთრი ფერის
ორბიტალები - თავისუფალი ორბიტალებია.