"ქიმიის უწყებანი" ტომი:5, ნომერი:1, 5-10 გვ.
იზოტოპების დაყოფა სპეციალიზებული მას-სპექტრომეტრის საშუალებით
საქართველოს აგრარული უნივერსიტეტი
რეზიუმე: იზოტოპების დაყოფის მას-სპექტრომეტრია არის სპეციალიზებული მეთოდი, რომელიც გამოიყენება იზოტოპების თანაფარდობის განსაზღვრისათვის კონკრეტულ ნივთიერებებში. ის საშუალებას გვაძლევს შევისწავლოთ სხვადასხვა ნივთიერება და მივიღოთ ინფორმაცია მისი გეოგრაფიული, ბიოლოგიური და ქიმიური წარმომავლობის შესახებ. სტატიაში განხილულია მეთოდის არსი და ამ ტექნიკის უპირატესობა სტანდარტულ მას-სპექტრომეტრიასთან, აგრეთვე სტატია მოგითხრობთ, მცენარეში იზოტოპური თანაფარდობის ჩამოყალიბების, ღვინის ხარისხის კონტროლისა და პროცესის ტექნიკური მხარის შესახებ.
საკვანძო სიტყვები: იზოტოპების დაყოფის მას-სპექტრომეტრია, იზოტოპების თანაფარდობა, კინეტიკური იზოტოპური ეფექტი, ფოტოსინთეზის პროცესი, ხარისხის კონტროლი
იზოტოპები ერთი და იმავე ატომთა სახესხვაობას წარმოადგენენ, რომელთაც გააჩნიათ ერთნაირი რაოდენობის პროტონი და განსხვავდებიან ნეიტრონების რიცხვით, რაც მათ განსხვავებულ მასას ანიჭებს. მათი არსებობა დაადგინა ორმა მეცნიერმა ერთმანეთისაგან დამოუკიდებლად, ესენი გახლავთ ფრედერიკ სოდი და კაზიმირ ფაიანსი, ქიმიის ისტორიის ფურცლებს კი დღემდე შემორჩა მათი სახელი დამსახურებულად, ფაიანსის და სოდის წესის სახელწოდებით, რომელიც გვიჩვენებს რადიაქტიური დაშლის ტიპებს.
მოგეხსენებათ, ატომები შეიძლება იყოს სტაბილური და არასტაბილური ანუ რადიაქტიური, როგორც სიტყვა გვეუბნება, ასეთი ატომები ასხივებს ენერგიას, მანამ, სანამ იგი არ მიაღწევს სტაბილურ მდგომარეობას. პერიოდულობის სისტემაში 15 რადიაქტიური ელემენტი გვხდება, რომელთაგანაც საზოგადოებისათვის ყველაზე მეტად ცნობილია: ურანი, პლუტონიუმი, პოლონიუმი. ამ უკანასკნელთა პოპულარობა განპირობებულია იმით, რომ მათ გამოყენება ჰპოვეს ბირთვულ იარაღში. მათი რადიაქტიური დაშლის შედეგად გარემოში გამოიყოფა კოლოსალური რაოდენობის ენერგია, რომელსაც დამანგრეველი ეფექტი გააჩნია. ასეთი ერთი ატომის დაშლას შეუძლია გამოიწვიოს მრავალი სხვა ატომის დაშლა, ე.წ ჯაჭვური რეაქციის წარმართვა. რადიაქტიური იზოტოპები აგრეთვე გამოიყენება გეოლოგიასა და არქეოლოგიაში, რადიომეტრული დათარიღების პროცესში, რომლის საშუალებითაც მეცნიერები შეისწავლიან ქანებისა და უძველესი ნაშთების ასაკს.
გარდა არასტაბილური იზოტოპებისა, არსებობს სტაბილური იზოტოპებიც, სხვანაირად მათ, სტაბილურ ნუკლიდებსაც უწოდებენ. შესაბამისად მათი შემცველობა ნივთიერებაში უცვლელი რჩება, რადგან ბუნებრივად არ განიცდიან დაშლას. ამ მიზეზის გამო, სტაბილური იზოტოპების რიცხვი მნიშვნელოვანი იარაღია სხვადასხვა ნივთიერების შესასწავლად [1].
იზოტოპების თანაფარდობის შესასწავლად გამოიყენება ხელსაწყო, რომლის სახელიცაა იზოტოპების თანაფარდობის მას-სპექტრომეტრი. ჩვეულებრივი მას-სპექტრომეტრისაგან განსხვავებით ის გვიჩვენებს ნუკლიდების თანაფარდობას. მეღვინეობასა და კვების ტექნოლოგიაში ყველაზე ხშირად მიმართავენ ნახშირბადისა და აზოტის იზოტოპების თანაფარდობების განსაზღვრას.
სანამ უშუალოდ გავეცნობოდეთ მეთოდის არსს, მანამ მიმოვიხილოთ ხელსაწყოს ქსელური სტრუქტურა. იგი შედგება, აირების წყაროს, ელემენტური ანალიზატორის, უნივერსალური აირების უწყვეტი ნაკადის მოწყობილობისაგან, ძირითადი ნაწილია მას-სპექტრომეტრი, სადაც ხდება იზოტოპური დაყოფა. მოძრავ ფაზად გამოიყენება ინერტული აირი. ამასთანავე, აუცილებელი აირია შესადარებელი სტანდარტი, წინასწარ ცნობილი იზოტოპური თანაფარდობით და აირადი ჟანგბადი, რომელიც გამოიყენება წვის პროცესისათვის. ნიმუშის ელემენტურ ანალიზატორში მოთავსების შემდეგ ის გადაადგილდება, აირების უწყვეტი ნაკადის მოწყობილობაში, რომელიც ახდენს ნივთიერების რაოდენობის ავტომატიზებულ შერჩევას, ნიმუშისა და შესადარებელი სიგნალის თანხვედრას და მას-სპექტომეტრისაკენ გაგზავნას (სურათი 1), სადაც ხდება მისი იონიზაცია.
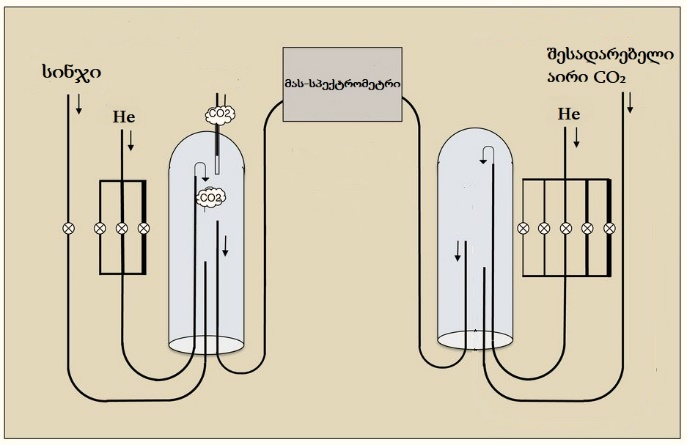
სურათი 1. აირების უწყვეტი ნაკადის მოწყობილობის მოქმედების პრინციპი

სურათი 2. Thermo Scientific™ DELTA V™ Isotope Ratio Mass Spectrometer
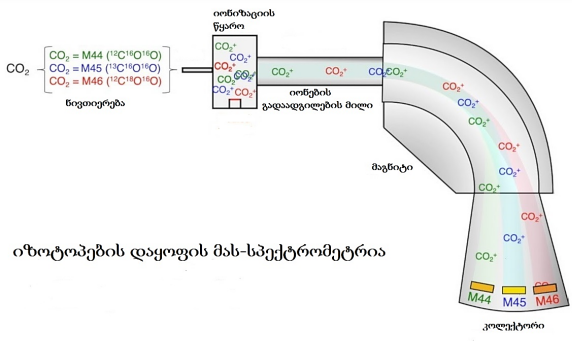
სხვა ტიპის მას-სპექტრომეტრები იზოტოპების თანაფარდობის განსაზღვრისათვის არ გამოდგება, რადგან მათ გააჩნიათ მხოლოდ ერთი კოლექტორი ანუ შემკრები, რომელიც ახდენს მხოლოდ კონკრეტული იზოტოპის დეტექტირებას, ხოლო იზოტოპების დაყოფის მას-სპექტრომეტრს გააჩნია რამდენიმე კოლექტორი, რომელსაც შეუძლია სხვადასხვა იზოტოპის განსაზღვრა ერთდროულად. იონიზირებული ნივთიერებები მაგნიტურ ველში მასა-მუხტის თანაფარდობის მიხედვით განაწილდებიან [2] (სქემა 1) , მძიმე იონები უფრო ნაკლებად გადაიხრებიან ველში, ხოლო მსუბუქი იონები ძლიერად და შესაბამისად პირველად მათი დეტექტირება მოხდება, ინფორმაცია გადამუშავდება კომპიუტერის საშუალებით, რომელიც იზოტოპების თანაფარდობას პიკის სახით გვიჩვენებს . ახლა წარმოვადგინოთ ხელსაწყოს ძირითადი ნაწილები (სურათი 2).
|
სქემა 1. იონების დაყოფის პრინციპი მას-სპექტრომეტრში
|
კაფსულაცია ანუ ნიმუშების მოთავსება ანალიზატორში ხდება სპეციალურად დამზადებული კალის კაფსულების საშუალებით, სადაც, პიპეტით თავსდება 1-2 მიკროლიტრი რაოდენობის საკვლევი სინჯი. (სურათი 3)
სურათი 3. კალის კაფსულა |
სურათი 4. კაფსულაციის ადგილი |
მთლიანი ნიმუში კალის კაფსულასთან ერთად იწვის 1020°C-ზე კვარცისაგან დამზადებულ საგანგებო ღუმელში [3] რომელიც ჩამონტაჟებულია ელემენტურ ანალიზატორში, მასში მოთავსებულია კობალტის ოქსიდისა და ქრომის ოქსიდის ნარევი (სურათი 5), რომელიც ნივთიერების დაშლის შედეგად მიღებული არასასურველი გაზების დაჟანგვას ახდენს, ის აგრეთვე შეიცავს სპილენძს, რომელიც სისტემას აშორებს ჭარბი რაოდენობის ჟანგბადს.
ყველაზე ხშირად ხდება ნახშირბადის იზოტოპების თანაფარდობის შესწავლა. ის გამოიყენება გეოქიმიაში, მედიცინასა და ბიოლოგიაში. სტაბილური იზოტოპების თანაფარდობას აღნიშნავენ ბერძნული ასოთი-დელტა, ხოლო თანაფარდობის გამოსახვა ხდება პრომილეებში.
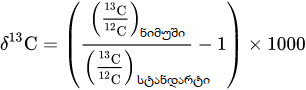
მეთოდის არსი მდგომარეობს შემდეგში: ჩვენ ვადარებთ ნიმუშის იზოტოპურ თანაფარდობას სტანდარტული აირის (ნახშირორჟანგი) იზოტოპურ თანაფარდობას. პროცესში გამოიყენება 100% ეთილის სპირტი, როგორ საკონტროლო ნივთიერება, რომლის იზოტოპური თანაფარდობის მნიშვნელობა დადგენილია IUPAC-ის მიერ, ის უდრის -26.91 პრომილეს , 0.07% ცდომილებაა დასაშვები, აღნიშნული სპირტი გამოიყენება იმ მიზნით, რომ დავადგინოთ თუ რამდენად გამართულად მუშაობს ხელსაწყო.
პროცესის არსს შევხედოთ, თუ კი გვსურს დავადგინოთ ღვინის ხარისხი, ღვინის სპირტში ვსაზღვრავთ δ13C-ს, მიღებულ შედეგს, ვადარებთ, იმავე, ნატურალური ყურძნისგან დამზადებულ ღვინის სპირტის იზოტოპურ თანაფარდობას, რომელიც ცნობილია და კონკრეტულ ზღვრებშია მოთავსებული. საქართველოს კანონმდებლობის მიხედვით, ყველა კატეგორიის ღვინოში ნახშირბადის C13/C12 იზოტოპის თანაფარდობა უნდა შეადგენდეს არანაკლებ –30 და არა უმეტეს –24 პრომილეს. შესაბამისად თუ კი ღვინის სპირტის იზოტოპური თანაფარდობა იქნება ამ ფარგლებს გარეთ, ის არ ჩაითვლება ნატურალურ ღვინოდ ანუ მასში შეტანილია სხვა მცენარეული პროდუქტის სპირტი, როგორიცაა: ხორბალი, სიმინდი, ჭარხალი და ა.შ. რაც უცვლის ღვინოს თავის ბუნებრივ იზოტოპურ თანაფარდობას. სხვადასხვა ქვეყნებს, ღვინის სპირტში ნახშირბადის იზოტოპების თანაფარდობის განსხვავებული რიცხვები აქვთ, რადგან იგი დამოკიდებულია ფიზიკურ პირობებზე, რომელშიც ხდება ვაზის გაზრდა [4]. ცხრილში მოცემულია ზოგიერთი ქვეყნის ღვინის სპირტში არსებული ნახშირბადის იზოტოპების თანაფარდობა, რომელიც წარმოადგენს ზღვრულ მნიშვნელობას, თუ კი ყურძნისაგან მიღებული ალკოჰოლური სასმელის δ13C შემცველობა მოთავსებულია ამ თანაფარდობებში, მაშინ ის ითვლება ხარისხიანად. (ცხრილი 1 )
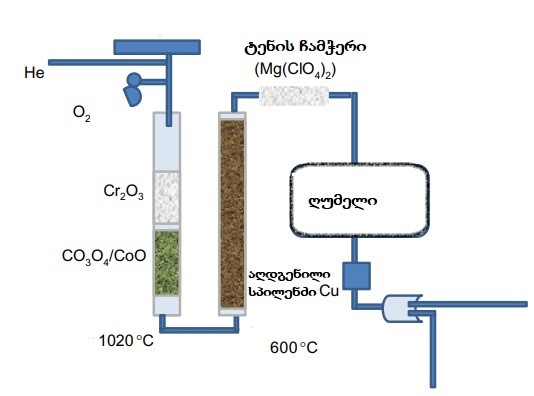
სურათი 5. ელემენტური ანალიზატორის შიდა სტრუქტურა
იზოტოპური თანაფარდობის ფორმირება დამოკიდებულია ბიოტურ და აბიოტურ ფაქტორებზე. აბიოტურ ფაქტორებს მიეკუთვნება ტემპერატურა, გეოგრაფიული წარმოშობა, პროდუქტის მოკრეფის დრო, მისი დამუშავება და ა.შ.
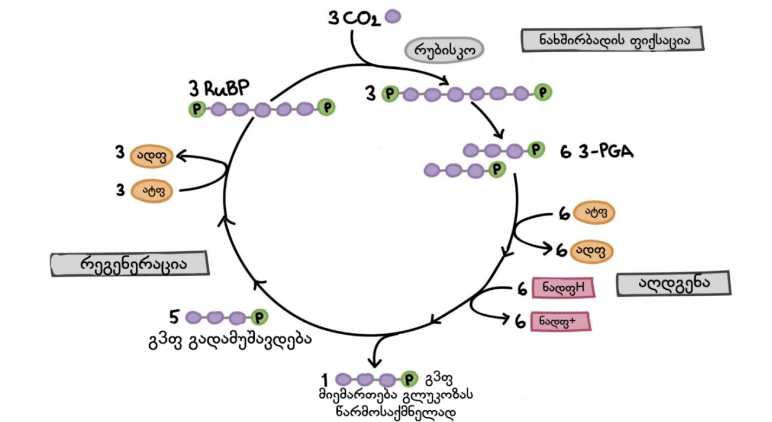
ბიოტური ფაქტორებიდან მნიშვნელოვანია, ნახშირორჟანგის ფიქსაცია ანუ ფოტოსინთეზის პროცესი. კალვინის ციკლის დროს (სურათი 4) ხდება ნახშირორჟანგის ფიქსაცია, CO2 უკავშირდება რიბულოზა 1,5-ბიფოსფატს და წარმოქმნის 3-ფოსფოგლიცერატს [5]. აღნიშნული რეაქცია გავლენას ახდენს იზოტოპური თანაფარდობის ჩამოყალიბებაზე მცენარეში, ანუ მას გააჩნია კინეტიკური იზოტოპური ეფექტი.
ცხრილი. იზოტოპების დასაშვები თანაფარდობა ღვინის სპირტში ქვეყნების მიხედვით
| C13/C12 იზოტოპების დასაშვები თანაფარდობა ღვინის სპირტში | |
| ავსტრალია | -26/-27 ‰ |
| ჩილე | -26/-28 ‰ |
| ჩინეთი | -25/-28 ‰ |
| ინდოეთი | -23/-27 ‰ |
| მაკედონია | -26/-28 ‰ |
| მექსიკა | -26/-27 ‰ |
| ახალი-ზელანდია | -27/-29 ‰ |
| სამხრეთ აფრიკა | -25/-28 ‰ |
| ტუნისი | -25/-26 ‰ |
| თურქეთი | -24/-26 ‰ |
მცენარეები, რომელთა შედგენილობაში შედის 3-ფოსფოგლიცერატი, აღნიშნავენ C3 აბრევიატურით, ასეთ მცენარეებში 13C იზოტოპის შემცველობა ნაკლებია, ვიდრე ატმოსფერულ ნახშირორჟანგში. ფოტოსინთეზის პროცესი შეიძლება წარიმართოს ჰეტჩისა და სლეკის გზითაც, C4 მექანიზმით, რა დროსაც ნახშირორჟანგს იკავშირებს ფოსფოენოლპირუვატი, წარმოქმნის რა ოქსალოაცეტატს, რომელიც იშლება მალისა და ასპარაგინის მჟავის მარილებად და საბოლოო მცენარე მდიდრდება 13C იზოტოპით. თუ რატომ მიდის ფოტოსინთეზის პროცესი სხვადასხვა გზით, ეს დამოკიდებულია მცენარის შედგენილობის თავისებურებაზე.
C3 მცენარეთა ჯგუფს მიეკუთვნება, ყურძენი და შაქრის ჭარხალი, ხოლო C4 ჯგუფს, ლერწმის შაქარი, სიმინდი და სხვა ზოგიერთი მარცვლეული. ზოგადად, იზოტოპური ეფექტის არსი მდგომარეობს, კონკრეტული ნუკლიდის მიერ რეაქციის სიჩქარეზე გავლენის მოხდენაში, რის გამოც, ამა თუ იმ ნივთიერების წარმოქმნა ხდება სწრაფად ან ნელა, რაც გავლენას ახდენს იზოტოპური თანაფარდობის წარმოქმნაზე.
|
სურათი 6. კალვინის ციკლი |
იზოტოპური თანაფარდობის განსაზღვრით შეგვიძლია დავადგინოთ ადრინდელ პოპულაციებში თუ რა დროის შემდეგ შეწყვიტა ბავშვმა ძუძუთი კვება და ჩაერთო კვებით ჯაჭვში. ახალშობილი, რომელიც იკვებება დედის რძით ის ღებულობს N-15 და O-18 იზოტოპებს დიდი რაოდენობით, როდესაც ის გადადის ხელოვნურ საკვებზე, იზოტოპების თანაფარდობის შემცირება ხდება ბავშვის ქსოვილებში, თუ სხვადასხვა ქსოვილში განვსაზღვრავთ მათ თანაფარდობას ცალკ-ცალკე ან ერთად, შეგვეძლება იმ დროის დადგენა როცა ბავშვი მოშორდა ძუძუთი კვებას [6]
გარდა ღვინისა, იზოტოპების თანაფარდობის განსაზღვრას დიდი როლი ენიჭება კვების ტექნოლოგიაში, მაგალითად თაფლის ნატურალურობის დადგენაში. C13/C12 ფარდობის განსაზღვრით ჩვენ შეგვიძლია ვთქვათ, არის თუ არა ის ჯანსაღი თუ მასში შეტანილია შაქრები დამატკბობლად. აგრეთვე იზიტოპების თანაფარდობის მას-სპექტრომეტრია გამოიყენება ზეთის, ყველის, ხორცის ხარისხის შესამოწმებლადაც. იზოტოპური თანაფარდობის განსაზღვრა მნიშვნელოვანი იარაღია აგრეთვე ქიმიურ ექსპერტიზაში [7] სხვადასხვა გამოძიების დროს ხდება, შარდსა და სხეულის ნაწილებში იზოტოპების ფარდობის შეფასება ნარკოტიკული ნივთიერებების აღმოსაჩენად, მისი გამოყენება ხდება ქიმიური მოწამვლის დროს ნივთიერებათა დასადგენად, ფეთქებადი ნაერთების შესასწავლად.
კიდევ ერთი მნიშვნელოვანი საკითხია, ცხოველთა მიგრაციის შესწავლა [8] რაც არ უნდა უცხოდ ჟღერდეს, მისი დადგენა შესაძლებელია იზოტოპური თანაფარდობის განსაზღვრით, ეს აგებულია შემდეგ პრინციპზე „რასაც ვჭამთ, იმას წარმოვადგენთ“. იზოტოპების ფარდობის განსაზღვრა ცხოველთა უჯრედებში ხდება, თუმცა მისი დადგენა ყველა ქსოვილში შეუძლებელია, რადგან ზოგიერთი მათგანი მეტაბოლურად აქტიურია, ზოგიერთი კი პასიური. კერატინის შემცველი ქსოვილები მეტაბოლურად ინერტულია, ასეთებია: თმა, ფრჩხილი, კლანჭი და ა.შ ამ ქსოვილებში იზოტოპური თანაფარდობის განსაზღვრა საშუალებას გვაძლევს წარმოდგენა ვიქონიოთ ცხოველთა სეზონურ გადაადგილებაზე. ანალოგიური დასკვნების გაკეთება შეიძლება წყალქვეშა სამყაროს ბინადართვისაც.
იზოტოპების დაყოფის მას-სპექტრომეტრია ერთ-ერთი აქტუალური მეთოდია ნივთიერებათა შესასწავლად, როგორც აღვნიშნეთ, მეთოდი გამოყენებას ჰპოვებს მეცნიერების სხვადასხვა დარგში და მის მიმართ ინტერესი ყოველდღიურად იზრდება. მეთოდი არის ზუსტი, მგრძნობიარე და ერთი ანალიზისათვის დროის მცირე მონაკვეთს მოითხოვს, გარდა ამისა, ის არ აბინძურებს გარემოს, არ გამოიყენება გარემოსათვის საშიში ნივთიერებები და იცავს მწვანე ქიმიის პრინციპს, თუმცა ხელსაწყო საკმაოდ ძვირადღირებულია და სასურველი იქნებოდა, რომ ხელმისაწვდომი იყოს ყველა ლაბორატორიისათვის, რაც ხელს შეუწყობდა მეცნიერების განვითარებას და უფრო მეტად საინტერესოს გახდიდა ლაბორატორიაში მუშაობს.
ლიტერატურა
[1] Zeland Muccio., Glen P. Jackson. Isotope ratio mass spectrometry. Analyst. 2009,134, 213-222.
[2] „About Isotope Ratio Mass Spectrometer“. https://acswebcontent.acs.org/ChemistryInContextSuite/applets/IsotopeRatioMassSpectrometry/about.html (უკანასკნელად გადამოწმებულია-2.22.2021)
[3] Carla Rodrigues., Rodrigo Maia., Marco Lauteri., Enrico Brugnoli. Stable isotope analysis Comprehensive Analytical Chemistry , 2013, 60:77-99.
[4] Norbert Christoph., Armin Hermann, Helmut Watcher. 25 Years authentication of wine with stable isotope analysis in the European Union. EDP Sciences. 2015, Volume 5, 02020.
[5] “The Calvin Cycle”
https://www.khanacademy.org/science/ap-biology/cellular-energetics/photosynthesis/a/calvin-cycle (უკანასკნელად გადამოწმებულია-2.22.2021)
[6] „What is stable isotope analysis?“. https://www.futurelearn.com/info/courses/archaeology/0/steps/15267 (უკანასკნელად გადამოწმებულია-2.22.2021)
[7] „Forensic Applications of Isotope Ratio Mass Spectrometry“. https://www.spectroscopyonline.com/view/forensic-applications-isotope-ratio-mass-spectrometry (უკანასკნელად გადამოწმებულია-2.22.2021)
[8] S. Zimmo., J. Blanco., Silke Nebel. The use of stable isotopes in the study of animal migration. Nature. 2012, 3(12):3.
გამოქვეყნებულია: 28-02-2021



