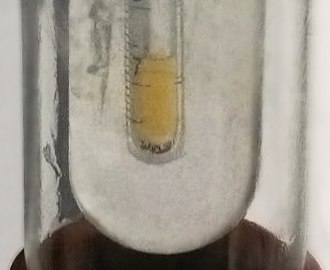
ფთორი
ფთორი ქიმიური ელემენტია ატომური ნორმით 9. იგი გამოისახება სიმბოლოთი F. ფთორი ელემენტალურ ფორმაში წარმოქმნის ორატომიან მოლეკულას F2, რომელშიც ელემენტები ერთმანეთთან ერთმაგი ბმით არიან დაკავშირებული . ფთორი ძალიან რეაქციისუნარიანი, მომწამლავი, მკრთალი მოყვითალო მოყავისფრო აირია. ელემენტალურ ფთორს აქვს ყველა ელემენტზე მაღალი ელექტროუარყოფითობა. ნახშირწყალბადები ადვილად იწვის ფთორის არეში ოთახის ტემპერატურაზე, განსხვავებით ჟანგბადის არესგან, რომლის ინიცირებას ნაპერწკლის შეტანა ესაჭიროება. მოლეკულური ფთორი ძალიან საშიშია, უფრო მეტად ვიდრე სხვა ჰალოგენები.
ფთორის მაღალი ელექტროუარყოფითობა და ატომის შედარებით მცირე რადიუსი მრავალ მის შენაერთს აძლევს უნიკალურ თვისებებს. მაგალითად, გამდიდრებული 235U (ძირითადი ბირთვული საწვავი) გადადის აქროლად UF6-ში. ასევე უნდა აღინიშნოს, რომ ნახშირბად-ფთორ ბმა ყველაზე მტკიცე ბმაა ორგანულ ნაერთებში. ეს ხელს უწყობს ფთორორგანული ნაერთების სტაბილურობას და მდგრადობას, მაგალითად, როგორიცაა PTFE/(ტეფლონი) და PFOS (პერფთოროქტანსულფომჟავა). ნახშირბად-ფთორ ბმის ინდუქციური ეფექტი გავლენას ახდენს მრავალი ფთორჩანაცვლებული მჟავების სიძლიერეზე. მაგალითის სახით შეიძლება დასახელდეს ტრიფლიკ მჟავა (ტრიფთორმეთან სულფომჟვა) და ტრიფთორძმარმჟავა. ფარმაცევტულ პრეპარატებში ხშირად შეჰყავთ ფთორი მეტაბოლიზმის პრევენციისათვის.
ისტორია
მინერალი ფლუორიტი (მინდვრის შპატი), ძირითადად შეიცავს კალციუმის ფთორიდს. იგი აღმოჩენილ იქნა 1530 წელს გ. აგრიკოლის მიერ. ფთორიდი გამოიყენებოდა როგორც ფლუქსი მეტალის ან მინერალის შესალღობად. სახელწოდება ფთორი ბერძნულად ნიშნავს დაშლას. 1670 წელს შვანჰარდმა (Schwanhard) აღმოაჩინა, რომ როდესაც მინას ამუშავებდნენ მინდვრის შპატითა და მჟავას ნარევით, ხდებოდა მინის ”ამოჭმა”. კ. შეელემ, მოგვიანებით ჰ. დევიმ, გეი-ლუსაკმა, ა. ლავუაზიემ და სხვებმა, რომლებიც ატარებდნენ ექსპერიმენტს ფთორწყალბადმჟავაზე, ადვილად მიიღეს იგი ფლუორიტის ურთიერთქმედებით კონცენტრირებულ გოგირდმჟავასთან.
მაგრამ ელემენტალური ფთორი მისი მაღალი რეაქციისუნარიანობის გამო შემდგომ კიდევ დიდი ხნის განმავლობაში ვერ იქნა გამოყოფილი. მისი გამოყოფის პროცესის დამუშავება მიმდინარეობდა ძალიან ნელა, რადგანაც ფთორის მიღება შესაძლებელი იყო მხოლოდ ელექტროლიზით, ისიც ზუსტ პირობებში. კვლევებს ართულებდა ის გარემოებაც, რომ აირადი ფთორი (F2) მოქმედებდა ექსპერიმენტში გამოყენებულ მრავალ მასალასთან. 1886 წელს ელემენტური ფთორის გამოყოფის შესახებ მოხსენება გააკეთა ჰ. მუასანმა (Henri Moissan), რომელმაც 1906 წელს ნობელის პრემია მიიღო ქიმიის დარგში.
ფთორის მიღების პირველი საკმაოდ ვრცელი მოხსენება იყო წარმოდგენილი მანჰეტენის პროექტში, სადაც ნაჩვენები იყო, რომ ურანიუმჰექსაფთორიდი (UF6) შეიძლება გამოყოფილ იქნას ურანიუმის 235U და 238U იზოტოპებიდან. დღეისათვის, როგორც აირადი დიფუზიური, ისე აირადი ცენტროფუგირების პროცესი იყენებს აირად UF6-ს გამდიდრებული ურანის მისაღებად. მანჰეტენის პროექტში ნაჩვენები იქნა, რომ UF6 იშლება UF4 და F2. ამ უკანასკნელის მიერ გამოწვეული კოროზიული პრობლემების თავიდან აცილების მიზნით UF6-ის გამტარი მილები მთლიანად შეიფუთა მეტალური ნიკელით (მიღებული ნიკელის დიფთორიდი ფთორთან არ ურთიერთქმედებს).
გავრცელება
დიდი ქიმიური აქტივობის გამო ფთორი ბუნებაში მხოლოდ ნაერთების სახით გვხვდება. იგი ძირითადად გავრცელებულია მინერალ ფლუორიდის - CaF2 (მლღობი შპატი), კრიოლიტის - Na3AlF6, ფთორის აპატიტის 3Ca3(PO4)2 × CaF2 სახით. ფთორი შედის ძვლების და კბილების მინანქრის შემადგენლობაში.
ფთორორგანული ნაერთები ბუნებაში იშვიათია. მათ აქვთ სხვადასხვა ბიოლოგიური როლი. ყველაზე ცნობილია ფთორაცეტატი, რომელსაც იყენებენ მცენარეთა დაცვისათვის სარეველების საწინააღმდეგოდ ავსტრალიაში, ბრაზილიაში და აფრიკაში. ფთორის ნაერთების ნაკლებობა ან სიჭარბე ორგანიზმში იწვევს კბილების დაავადებას. მისი დეფიციტის დროს ვითარდება კარიესი, ხოლო სიჭარბისას - ფლუოროზი.
იზოტოპები
მიუხედავად იმისა, რომ ფთორს აქვს მრავალი იზოტოპი, მათგან მდგრადი მხოლოდ ერთი 19F იზოტოპია. დანარჩენებს აქვთ ძალიან მცირე ნახევარდაშლის პერიოდი და ამიტომ ბუნებაში არ გვხვდებიან. აქედან გამომდინარე, ფთორი მონოიზოტოპური ელემენტია.
18F - რადიოაქტიური იზოტოპია. მისი ნახევარდაშლის პერიოდია 110 წუთი. კომერციულად იგი წარმოადგენს პოზიტრონების წყაროს. მან ძირითადი გამოყენება ჰპოვა პოზიტრონების გამომმუშავებელ ტომოგრაფიულ სკანინგში.
ფიზიკური თვისებები
მოლეკულური ფთორი - F2 წარმოადგენს ღია ყვითელ ან ყავისფერ აირს. იგი რთულად თხევადდება. ფთორი ძლიერი დამჟანგველი აგენტია. იგი ყველა ელემენტზე უფო რეაქციისუნარიანია და აქვს ყველა ელემენტზე მეტი ელექტროუარყოფითობა -3.98 პაულის კლასიკური შკალის მიხედვით.
ქიმიური თვისებები
ფთორი წარმოქმნის ნაერთებს, სადაც მისი დაჟანგულობის ხარისხია -1, გამონაკლისია F2 , სადაც მისი დაჟანგულობის ხარისხია 0. ფთორი უკავშირდება კეთილშობილ აირებს - არგონს, კრიპტონს, ქსენონს და რადონს. ფთორი წყალბადს უერთდება აფეთქებით სიბნელეშიც კი. იგი ურთიერთქმედებს მეტალებთან, წყალთან, ასევე სხვა ნაერთებთან, რომლებიც ფთორის ნაკადში იწვიან კაშკაშა ალით. ფთორი სხვა ჰალოგენიდებისაგან განსხვავებულად ურთიერთქმედებს წყალთან - ფთორიანი წყალი არ მიიღება, რადგან წყალი იწვის ფთორში, წვის პროდუქტებია: ფთორწყალბადი, ჟანგბადი, ოზონი, ჟანგბადის ფთორიდი და წყალბადის პეროქსიდი.

ფლუორიტის (CaF2) კრისტალები
ფთორნაერთების ქიმია
ფთორი წარმოქმნის მრავალრიცხოვან ნაერთებს მისი მცირე ატომური რადიუსისა და კოვალენტური ბუნების გამო. ელემენტალური ფთორი ძლიერი დამჟანგველია. ფტორიდებში ფთორი დამუხტულია უარყოფითად. ფთორიდები წყალში გახსნისას იძლევიან ფთორიდ იონს, რომელიც ტოკსიკურია: ნატრიუმის ფთორიდის ლეტალური დოზა 70კგ ცოცხალ ორგანიზმზე შეადგენს 5-10 გ-ს. ფთორის შენაერთები მეტალთან სტაბილურია. წყალბადთან იძლევა ფთორწყალბადს, რომელიც აირადი ნაერთია. წყალბადური ბმის გამო იგი 19.5°C ტემპერატურაზე დაბლა თხევადდება. ფთორწყალბადი იხსნება წყალში ნებისმიერი თანაფარდობით. ფთორწყალბადი სხვა ჰალოგენწყალბადმჟავებზე სუსტი მჟავაა და მიეკუთვნება საშუალო მჟავებს. მჟავების სიძლიერე იზრდება რიგში HF<HCl<HBr<HI, რაც აიხსნება H-Hal ბმის ენერგიის შემცირებით. ფთორწყალბადმჟავას მნიშვნელოვან თვისებას წარმოადგენს სილიციუმ (IV) ოქსიდთან ურთიერთქმედება.
SiO2 + 4HF → SiF4 + 2H2O
SiF4 + 2HF→ H2(SiF6)
იგი შლის მინას, რადგან ურთიერთქმედებს მინაში შემავალ SiO2-თან.ამიტომაც იგი ცნობილია მლღობი მჟავას სახელწოდებით. ამ რეაქციას იყენებენ მინაზე წარწერის გასაკეთებლად.
ტუტე მეტალთა ფთორიდების წყალხსნარებს აქვთ ფუძე თვისება. მაგალითად, 1 მოლი NaF-ის წყალხსნარის pH = 8.59,ხოლო 1მოლი NaOH (ძლიერი ფუძე) pH = 14.00.
ფთორორგანული ნაერთები
კოვალენტური ფთორ-ნახშირბად ბმა ძალიან სტაბილურია. ამის მაგალითია ფთორნახშირბადის პოლიმერი - პოლიტეტრაფთორეთენი (ტეფლონი), რომელიც წარმოადგენს თერმომდგრად და წყალმედეგ პოლიმერს და გამოიყენება საყოფაცხოვრებო ნივთების (ტაფების, ქვაბების) დასამზადებლად.
ორგანოფთორიდები შეიძლება გამოყენებულ იქნას როგორც სამკურნალო პრეპარატები.
მიღება
წარმოებაში ფთორი მიიღება ფთორწყალბადის ელექტროლიზით კალიუმის ფთორიდის თანაობისას. აირადი ფთორი წარმოიქმნება ანოდზე, ხოლო კათოდზე მიიღება აირადი წყალბადი. ამ პირობებში კალიუმის ფთორიდი (KF) გადადის კალიუმის ბიფთორიდში (KHF2), რომელიც აქტიური ელექტროლიტია.
HF + KF → KHF2
2 KHF2 → 2 KF + H2 + F2
ფოსფატ შემცველი მინერალები მნიშვნელოვანი რაოდენობით შეიცავენ კალციუმის ფთორიდს ფლუორიტის სახით. ეს მინერალები გოგირდმჟავასთან ურთიერთქმედებით იძლევიან ფთორწყალბადს:
CaF2 + H2SO4 → 2 HF + CaSO4
1986 წელს ფთორის აღმოჩენის ასი წლისთავის იუბილეს აღსანიშნავ კონფერენციაზე კარლ ქრისტის მიერ წარმოდგენილ იქნა ფთორის ქიმიურად მიღების გზა უწყლო HF-ის ხსნარში K2MnF6 და SbF5-ის ურთიერთქმედებით 150°C-ზე.
2 K2MnF6 + 4 SbF5 → 4 KSbF6 + 2 MnF3 + F2
ამ მოხსენებამ უჩვენა, რომ ელემენტის მისაღებად ელექტროლიზი არ არის ერთადერთი გზა.
გამოყენება
ატომური და მოლეკულური ფთორი გამოიყენება ნახევარგამტარების, სახლის პანელების და MEMS (მიკროელექტრომექანიკური სისტემების) წარმოებაში. იმავე მიზნებისათვის შეიძლება გამოყენებულ იქნას აგრეთვე ქსენონდიფთორიდი.
ფთორწყალბადმჟავა (HF) გამოიყენება მინების გრავირებისათვის.
ტეტრაფთორეთილენი და პერფთოროქტანოილმჟავა (PFOA) უშუალოდ გამოიყენებიან ტეფლონის (პოლიტეტრაფთორეთილენის) მისაღებად.
ფთორი არაპირდაპირი გზით გამოიყენება ფრეონის წარმოებაში. ქლორფთორნახშირბადები (CFCs) გამოიყენება ჰაერის კონდინცირებისათვის და მაცივრებში.
ფთორი გამოიყენება სუფთა ურანის მისაღებად .ურანფთორიდიდან და აგრეთვე გამოიყენება მრავალი კომერციული ფთორრეაგენტების, მათ შორის ფარმაცევტული, აგროქიმიური ნაერთების, საპოხი ნაერთების და ტექსტილის წარმოებაში. მაღალი კონცენტრაციით ნატრიუმის ფთორიდი (NaF), შეიძლება გამოყენებულ იქნას როგორც ინსექტიციდი, განსაკუთრებით ტარაკანების წინააღმდეგ.
ნატრიუმჰექსაფთორალუმინატებს (კრიოლიტი) იყენებენ ელექტროლიზით ალუმინის მისაღებად.
ფთორის არაორგანული ნაერთები ნატრიუმის ფთორიდი (NaF) და კალის დიფთორიდი (SnF2) გამოიყენებიან კბილის პასტებში კბილის კარიესის პრევენციისათვის.
დაახლოებით ორმოცდაათამდე ფარმაცევტული და 30%-მდე აგროქიმიური ნაერთი შეიცავს ფთორს. ზოგადი ანესთეზიის ბევრი მნიშვნელოვანი აგენტი - სევოფთორინი, დესფთორანი და იზოფთორანი წარმოადგენენ ფთორნახშირწყალბადების წარმოებულებს.
ფთორირებული დექსამეტაზონი და ტრიამსინოლონი მიეკუთვნება სინთეზური კორტიკოსტეროიდების კლასს.
ფთოროქინოლონები წარმოადგენენ ფართო სპექტრის ანტიბიოტკს.
რადიოაქტიური იზოტოპი 18F-ის შემცველი ნაერთები ხშირად გამოიყენება, როგორც პოზიტრონის გამომყოფი ტოპოგრაფი, რადგანაც მისი ნახევარდაშლის პერიოდი (110 წთ) სტანდარტულ პოზიტრონ გამომყოფზე უფრო ხანგრძლივია.
ფთორის ძირითდი იზოტოპი 19F ინერტული ფთორირებული აირის ან სითხის ფორმით გამოიყენება, როგორც ნიმუში (ნიშანდებული) ბირთვი MRI.
მასალა მომზადებულია www.wikipedia.com -ის მიხედვით