კობალტი
კობალტი წარმოადგენს მაგარ, მბრწყინავ, რუხი ფერის მეტალს. მისი სიმბოლოა Co, ატომური ნომერი 27. კობალტის საფუძველზე მიღებული ფერები და პიგმენტები უძველესი დროიდან გამოიყენება ძვირფას ქვებში, საიუველირო ნაწარმებსა და მხატვრობაში.
კობალტი გვხვდება სხვადასხვა, მეტალური ბზინვარების მინერალებში, მაგალითად კობალტინში (CoAsS). მაგრამ იგი ძირითადად მიიღება, როგორც სპილენძისა და ნიკელის თანამდევი პროდუქტი. დიდი რაოდენობით კობალტს ღებულობენ კონგოს დემოკრატიულ რესპუბლიკაში და ზამბიაში.
კობალტი გამოიყენება მაგნიტური მდგრადი და გამძლე შენადნობების მისაღებად. სმალიტები (კობალტ სილიკატური მინა) და კობალტის ლურჯი (კობალტ (II) ალუმინიტი, CoAl2O4) მინებს აძლევს მკვეთრ, ღრმა ლურჯ შეფერვას. კობალტის ლურჯს ასევე იყენებენ კერამიკის, მელნის, საღებავებისა და ლაქების ტექნოლოგიაში.
კობალტი არის აუცილებელი ელემენტი ცხოველთა ორგანიზმისათვის, როგორც კობალტმინკოენზიმის აქტიური ცენტრი. იგი შეიცავს ვიტამინ B12, რომელიც აუცილებელია ძუძუმწოვრებისათვის. კობალტი აგრეთვე წარმოადგენს ბაქტერიების და სოკოების აქტიურ მკვებავ ელემენტს.
ისტორია
კობალტის შენაერთებს საუკუნეების განმავლობაში იყენებდნენ მუქი ლურჯი შეფერილობის მისაცემად მინების, ჭიქურების და კერამიკისათვის. კობალტი ჩვენს ერამდე სამი ათასი წლის წინ იქნა აღმოჩენილი ეგვიპტეში, სპარსეთში და ჩინეთში.
კობალტი პირველად აღმოაჩინა შვედმა ქიმიკოსმა გ. ბრანდტმა 1735 წელს. მან შეძლო ეჩვენებინა, რომ მინის ლურჯი შეფერვა გამოწვეული იყო კობალტის არსებობით. სიტყვა კობალტი წარმოდგა გერმანული სიტყვისაგან ”kobalt”. ”kobold” ნიშნავს "goblin"-ს (ფუძის, სახლის ანგელოზს), მე-19 საუკუნეში კობალტს დიდი რაოდენობით აწარმოებდნენ ნორვეგიაში (მსოფლიო წარმოების 70-80%).
გავრცელება
კობალტის მდგრადი ფორმა წარმოიქმნება უახლოეს ვარსკვლავ ასტრონზე. კობალტი დედამიწის ქერქის 0.0029% შეადგენს.
კობალტი გვხვდება სპილენძისა და ნიკელის მინერალებში. აგრეთვე შეიძლება არსებობდეს გოგირდთან და დარიშხანთან ერთად კომბინაციაში.
მას ვხვდებით ისეთ მინერალებში, როგორიცაა კობალტინი (CoAsS), საფლორიტი (CoAs2), სკუთერედიტი (CoAs3) და გლაუკოდიტი.
მინერალი კათერიტი მსგავსია პირიტის და გვხვდება სპილენძის დეპოზიტში. ატმოსფეროში სულფიდური მინერალები იჟანგებიან და გადადიან ვარდისფერ ერითრიტში (”კობალტის კრიალა”: Co3(AsO4)2·8H2O) და სფეროკობალტიტი (CoCO3).
იზოტოპები
59Co წარმოადგენს კობალტის ერთადერთ სტაბილურ იზოტოპს და ასევე ერთადერთ იზოტოპს, რომელიც ბუნებაში არსებობს. დახასიათებულია კობალტის 22 რადიოიზოტოპი, რომელთაგან ყველაზე სტაბილურია 60Co - ნახევარდაშლის პერიოდით 5.2714 წელი, 57Co - ნახევარდაშლის პერიოდით 271.79 დღე, 56Co - ნახევარდაშლის პერიოდით 77.27დღე და 58Co - ნახევარდაშლის პერიოდით 70.86 დღე. ყველა დანარჩენი რადიოიზოტოპის ნახევარდაშლის პერიოდი 18 საათზე ნაკლებია, მათგან უმეტესობის ნახევარდაშლის პერიოდი 1 წმ-ზე ნაკლებია. ამ ელემენტს აგრეთვე აქვს ოთხი მეტა მდებარეობა, მათი ნახევარდაშლის პერიოდი 15 წუთზე ნაკლებია.

ელექტროქიმურად მიღებული 99.9% სისუფთავის კობალტი
ფიზიკური თვისებები
კობალტი ფერომაგნიტური მეტალია სპეციფიური მიზიდულობით 8.9 (20°C). იგი წარმოადგენს მკრთალი ყვითელი ფერის მეტალს ვარდისფერი ან ლურჯი ელფერით. ბუნებაში სუფთა კობალტი არ არის ნაპოვნი, მაგრამ მისი ნაერთები საკმაოდ გავრცელებულია.
კობალტის კიურის ტემპერატურაა 1115°C, ხოლო მაგნიტური მომენტია 1.6-1.7.
ქიმიური თვისებები
კობალტი სუსტი აღმდგენი მეტალია. ჰაერზე იჟანგება და სხვა მეტალების მსგავსად იფარება პასიური ოქსიდის ფენით. იგი ურთიერთქმედებს ჰალოგენებთან და გოგირდთან. ჟანგბადში გაცხელებით იძლევა Co3O4, რომელიც 900°C-ზე კარგავს ჟანგბადს და გადადის მონოქსიდში CoO.
კობალტის ჟანგვითი რიცხვია +2 და +3, თუმცა ცნობილია ნაერთები ჟანგვითი რიცხვით -3-დან +4-ის ჩათვლით. კობალტ (II) მარილები წყალხსნარებში წარმოქმნიან მოვარდისფრო-წითელ კომპლექსს [Co(H2O)6]+2. ქლორიდის დამატება იძლევა ინტენსიური ლურჯი ფერის კომპლექსს [CoCl4]-2.
ქიმიური თვისებები
ჟანგბად და ქალკოგენ ნაერთები
ცნობილია კობალტის რამდენიმე ოქსიდი. მწვანე კობალტ(II) ოქსიდს (CoO) აქვს ქვამარილის სტრუქტურა. იგი ადვილად იჟანგება წყალში ჟანგბადით და იძლევა კობალტ(III) ჰიდროქსიდს - (CoO(OH)).
600–700 °C-ზე CoO იჟანგება ლურჯი ფერის კობალტ (II, III) ოქსიდამდე (Co3O4), რომელსაც ფერომაგნიტური რკინის სტრუქტურა აქვს. აგრეთვე ცნობილია შავი კობალტ(III) ოქსიდი (Co2O3). კობალტის ოქსიდები არიან ანტიფერომაგნიტურები დაბალ ტემპერატურაზე: CoO (ნეელის ტემპერატურა 291 K) და Co3O4 (ნეელის ტემპერატურა 40 K), სადაც იგი მაგნეტიტის (Fe3O4) ანალოგიურია, რომელშიც კობალტის ჟანგვითი რიცხვი +2 და +3 ერთად.
-chloride-hexahydrate-sample.jpg)
კობალტ (II) ქლორიდის ჰექსაჰიდრატი
კობალტის ქალკოგენიდებია შავი კობალტ(II) სულფიდი CoS2, რომელსაც პირიტის მსგავსი სტრუქტურა აქვს და Co2S3. პენტლენდიტი (Co9S8) არის მეტალით მდიდარი ნაერთი.
ჰალოგენიდები
ცნობილია კობალტის ოთხი დიჰალოგენიდი: კობალტ(II) ფთორიდი (CoF2, ვარდისფერი), კობალტ(II) ქლორიდი (CoCl2, ლურჯი), კობალტ(II) ბრომიდი (CoBr2, მწვანე), კობალტ(II) იოდიდი (CoI2, მუქი ლურჯი). ეს დიქლორიდები არსებობენ, როგორც უწყლო , ისე ჰიდრატების სახით. ამასთან უწყლო დიქლორიდები ლურჯი ფერისაა, ხოლო ჰიდრატები წითელი. კობალტ(III)-ის მცირერიცხოვან მდგრად მარტივ ნაერთებს შორის ერთ-ერთია კობალტ(III) ფთორიდი. იგი გამოიყენება ფთორირების ზოგიერთ რეაქციაში, წყალთან რეაგირებს ენერგიულად.
კოორდინაციული ნაერთები
სხვა მეტალების მსგავსად, კობალტიც წარმოქმნის კოორდინაციულ ნაერთებს. მაგალითად, Co+3 იონებს აქვთ მიდრეკილება წარმოქმნან კომპლექსები ამინის ლიგანდთან. ფოსფინის ლიგანდი ცდილობს დაიკავშიროს Co+2 და Co+. ამის მაგალითს წარმოადგენს ტრის(ტრიფენილფოსფინ) კობალტ(I)-ის ქლორიდი ((P(C6H5)3)3CoCl).
ოქსიდსა და ქლორიდს შეუძლიათ Co4+ წარმოებულების სტაბილიზირება, მაგალითად კოენზიმი ჰექსაქლორკობალტატი (Cs2CoF6)) და კალიუმის პერკობალტატი (K3CoO4).
ალფრედ ვერნერი, ნობელის პრემიის გამარჯვებული კოორდინაციულ ქიმიაში, მუშაობდა ნაერთებზე, ემპირიული ფორმულით CoCl3(NH3)6. განსაზღვრული იქნა კობალტ(III) ჰექსამინქლორიდის ერთ-ერთი იზომერი. ეს კოორდინაციული კომპლექსი ”ტიპიური” ვერნერის ტიპის კომპლექსია. იგი შეიცავს ექვსი ამინის ლიგანდის მიერ კოორდინაციულ ცენტრალურ კობალტის ატომს, რომლებიც ერთმანეთის მიმართ განლაგებულნი არიან ორთოგონალურად, სადაც მოპირდაპირედ განლაგებულია სამი ქლორიდ ანიონი.
მეტალორგანული ნაერთები. კობალტოცენი წარმოადგენს ფეროცენის მდგრად ანალოგს. კობალტკარბონილი (Co2(CO)8) წარმოადგენს კარბონილირების რეაქციის კატალიზატორს. ვიტამინი B12 არის იშვიათი მეტალოორგანული ნაერთი, რომელიც ნაპოვნია ბუნებაში. იგი ერთადერთი ვიტამინია, რომელიც შეიცავს მეტალის ატომს.

კობალტის წიაღისეული
.png)
კობალტის მოპოვება 2005 წელს
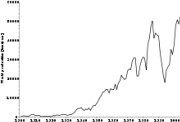
კობალტის წარმოება მსოფლიო მასშტაბით
მიღება
2005 წელს კატანგის პროვინციაში (კონგოს დემოკრატიული რესპუბლიკა), სპილენძის დეპოზიტის დამუშავებით ღებულობდნენ კობალტს, რომელიც შედგენს მსოფლიო წარმოების დაახლოებით 40%.
სპილენძისა და ნიკელისაგან კობალტის გამოყოფის რამდენიმე მეთოდი არსებობს, რაც დამოკიდებულია გამოყენებული საბადოს შემადგენლობაზე და კობალტის კონცენტრაციაზე. საბადოდან კობალტის გამოყოფის ერთ-ერთი საფეხური მოიცავს ქაფის ფლოტაციას, რომელშიც ხდება, სხვადასხვა მადნის კომპონენტების დაკავშირება, რასაც მივყავართ კობალტის მადნის გამდიდრებამდე. შემდგომი გაცხელებით საბადო გადადის კობალტის სულფიდში, მაშინ როცა სპილენძი და რკინა იჟანგება ოქსიდამდე. შემდგომ ახდენენ წყალხსნარის ექსტრაქტიდან სულფატის და არსენატის ერთად გამოტუტვას. ნალექს ამუშავებენ გოგირდმჟავით და იღებენ სპილენძის სულფატის ხსნარს. კობალტი ასევე შეიძლება მიღებულ იქნას სპილენძის ნალღობის შლაკების გამოტუტვით.
ზემოთ აღნიშნული პროცესის დროს პროდუქტები გარდაიქმნებიან კობალტის ოქსიდად (Co3O4), რომელსაც შემდეგ აღადგენენ ალუმინოთერმიით ან აღადგენენ ნახშირით ბრძმედებში.

ადრეული ხანის ჩინური ლურჯი და თეთრი ფაიფურის ნაკეთობა, დამზადებული 1335 წელს
გამოყენება
კობალტი, როგორც მეტალი ძირითადად გამოიყენება შენადნობების სახით. მათგან ამზადებენ ცეცხლგამძლე მასალებს, გაზის ტურბინებს და საავიაციო-საინჟინრო მასალებს. ერთ-ერთი ასეთი შენადნობია ვიტალუმი (65% Co, 28% Cr, 3% W და 4% Mo), რომელიც არ განიცდის კოროზიას 800-850 °C-მდე. მყარი შენადნობები - სტელიტები (40-60% Co, 20-35% Cr, 5% W და 1-2% C) გამოიყენება მჭრელი ინსტრუმენტების დასამზადებლად.
როგორც უჟანგავ ლითონს, კობალტს იყენებენ ფოლადისა და რკინის ნაკეთობების დასაფარავად (მოკობალტება). კობალტი ასევე შედის კერამიკომეტალური, მყარი შენალღობების შემადგენლობაში (კერმეტები).
კობალტის ნაერთები მინას აძლევენ მუქ ლურჯ შეფერვას (კობალტის სილიკატის წარმოქმნის გამო). ასეთი მინები დანაყული ფხვნილის სახით გამოიყენება ”სმალტების” ან ”კობალტას” სახელით ლურჯ საღებრებში. ”სმალტები” წარმოადგენს მინერალ სმალტიტის კვარცისა და კალიუმის კარბინატის ნალღობის ნარევს, რომელიც სილიკატურ მინას აძლევს მუქ ლურჯ შეფერვას.
შუა საუკუნეებში (1780, 1802) აღმოჩენილი იქნა კობალტ-მწვანე და კობალტ-ლურჯი. ეს ორი ფერი - კობალტ-ლურჯი (კობალტის ალუმინატი) და კობალტ-მწვანე (კობალტ(II) ოქსიდისა და თუთიის ოქსიდის ნარევი) გამოიყენებოდა როგორც პიგმენტები.
კობალტის შენადნობები, როგორც ზემოთ აღვნიშნეთ მდგრადია კოროზიის მიმართ. სპეციალური კობალტ-ქრომ-მოლიბდენის შენალღობი გამოიყენება თეძოსა და მუხლის პროტეზირებაში, აგრეთვე გამოიყენება კბილის პროტეზებში (ნიკელის მიმართ ალერგიის თავიდან აცილების მიზნით). ზოგიერთი ხარისხის ფოლადში კობალტს ამატებენ ტემპერატურისა და ატმოსფეროს მიმართ გამძლეობის გასაზრდელად. ალუმინის, ნიკელის, კობალტის და რკინის სპეციალური შენადნობი (ცნობილი ალნიკოს სახელწოდებით) და სამარიუმი და კობალტი (სამარიუმ-კობალტის მაგნეტი) გამოიყენებიან მუდმივ მაგნიტებში.
ლითიუმ-კობალტ ოქსიდი (LiCoO2) ფართოდ გამოიყენება ლითიუმ იონის შემცველი ბატარეების ელექტროდებში. ნიკელ-კადმიუმი (NiCd) და ნიკელ-მეტალჰიდრიდი (NiMH) ბატარეები აგრეთვე მნიშვნელოვნად შეიცავენ კობალტს.
კობალტის სხვადასხვა ნაერთებმა გამოყენება ჰპოვა კატალიზური ჟანგვის რეაქციებში. კობალტის აცეტატი იხმარება ქსილოლის ტერეფტალმჟავად გარდაქმნის დროს, რომელიც წარმოადგენს პრეკურსორს პოლიეთილენტერეფტის პოლიმერის მისაღებად. კობალტის კარბოქსილატები წარმოადგენენ ტიპიურ კატალიზატორებს (ცნობილია კობალტის საპნების სახელწოდებით). ისინი აგრეთვე გამოიყენებიან ლაქებში და მელნებში, როგორც ”მშრალი აგენტები” მშრალი ზეთების დაჯანგვისას. იგივე კარბოქსილატები გამოიყენება ფოლადის ადგეზიური თვისებების გასაუმჯობესებლად. კობალტის ბაზაზე არსებულ კატალიზატორებს აგრეთვე დიდი მნიშვნელობა აქვთ ნახშირბადის მონოქსიდისათვის დამახასიათებელ რეაქციებში. კობალტი გამოიყენება ფიშერ-ტროპშის რეაქციებში კატალიზატორად. კერძოდ გამოიყენება ნახშირბადის მონოქსიდის ჰიდროგენიზაციის რეაქციებში, სადაც ეს უკანასკნელი გარდაიქმნება თხევად საწვავად. ალკანების ჰიდროფორმილირების დროს ხშირად კატალიზატორად იყენებენ კობალტის ოქტაკარბონილს.
ბენზინის ჰიდროდესულფირების პროცესში კატალიზატორად გამოიყენება კობალტისა და მოლიბდენის ნაწარმები. ეს პროცესი ხელს უწყობს ბენზინის გასუფთავებას გოგირდის მინარევებისაგან, რომელიც წარმოადგენს ხელის შემშლელ ფაქტორს თხევადი საწვავის გასუფთავების დროს.
60Co იზოტოპი მედიცინაში და ტექნიკაში აგრეთვე გამოიყენება, როგორც g-გამოსხივების წყარო.
ბიოლოგიური როლი
კობალტი მცირე რაოდენობით წარმოადგენს ცოცხალი ორგანიზმისათვის აუცილებელ ელემენტს. კობალტის ხსნადი მარილებისათვის LD50-ს წარმოადგენს 150-დან 500მგ/კგ. მაგალითად, 100კგ. წონის ადამიანის LD50 შეადგენს დაახლოებით 20 გრამს.
ძუძუმწოვრებს ესაჭიროება კობალტის მცირე რაოდენობა, რომელსაც ისინი ღებულობენ ვიტამინ B12-ის ბაზაზე. კობალტ-60 წარმოადგენს კობალტის ხელოვნურ რადიოაქტიურ იზოტოპს, იგი არის მნიშვნელოვანი რადიოაქტიური თრეისერი და გამოიყენება როგორც ანტიკანცეროგენური აგენტი.
1966 წელს, კანადაში, ლუდის ქაფის სტაბილიზაციისათვის დაამატეს კობალტის ნაერთები, რამაც გამოიწვია კარდიომიოპატია, რომელიც ამის შემდეგ ცნიბილია როგორც ”ლუდის მსმელების კარდიომიოპატია ”.
მასალა მომზადებულია www.wikipedia.com -ის მიხედვით



