ოქრო
ქიმიური ელემენტი ოქრო აღინიშნება სიმბოლოთი Au (ლათ. Aurum, "აურორა" - დილის აისი). მისი ატომური ნომერია 79. იგი რბილი და ძლიერ პლასტიკური, მბზინვარე ყვითელი ფერის ლითონია. მოთავსებულია ქიმიურ ელემენტთა პერიოდულობის სისტემის მეთერთმეტე ჯგუფში.
ოქრო ძვირფასი ლითონია და გამოიყენება მონეტების, საიუველირო ნაწარმის და ხელოვნების სხვადასხვა ნიმუშის დასამზადებლად ხელნაწერი ისტორიის დასაწყისიდანვე.
ოქრო გვხვდება თვითნაბადი სახით. სუფთა ოქროს კაშკაშა ყვითელი ფერი და ელვარება აქვს და ტრადიციულად ითვლება მომხიბვლელად, რასაც იგი აღწევს კოროზიისადმი მდგრადობით ჰაერსა თუ წყალში. ოქრო მიჩნეულია სიმდიდრის სიმბოლოდ და დაგროვების ობიექტია. იგი საყოველთაო ფულის ეკვივალენტის ფუნქციასაც ასრულებს. ოქროს სტანდარტები განსაზღვრავს მონეტარული პოლიტიკის საფუძვლებს. ოქროს მრავალგვარი სიმბოლური და იდეოლოგიური დატვირთვაც აქვს.

თვითნაბადი ოქრო

თვითნაბადი ოქრო კვარცის ნაწიკალებზე
ოქრო პირველადად გამოიყენება დაგროვების ობიექტად, თუმცა შემდეგ ჰპოვა მრავალი ინდუსტრიული დანიშნულებაც (მაგ. სტომატოლოგიასა და ელექტრობაში). ოქროს ინდუსტრიული მიზნებით გამოყენების მიზეზია მისი განსაკუთრებული მდგრადობა ოქსიდური კოროზიისადმი და შესანიშნავი ელექტროგამტარობა.
ქიმიური თვალსაზრისით ოქრო გარდამავალი ლითონია, რომელიც ამჟღავნებს სხვადასხვა ვალენტობას განსხვავებულ სიტუაციებში. სუფთა ოქრო ნაკლებად რეაქტიულია, თუმცა რეაქციაში შედის სამეფო არაყთან (მჟავების კომბინაცია), მაგრამ არა ცალკეულ მჟავებთან. იხსნება ციანიდებში. ოქრო ასევე იხსნება ვერცხლისწყალში და წარმოქმნის ამალგამას ფენებს, თუმცა მასთან რეაქციაში არ შედის. ოქრო მდგრადია აზოტმჟავის მიმართ, რომელიც ურთიერთქმედებს ვერცხლთან და სხვა მრავალ ლითონთან.
ისტორია
ადამიანი ოქროს უხსოვარი დროიდან მოიპოვებს. ოქროს კაცობრიობა უკვე ნეოლითის ხანაში (V ს. ჩ.წ.ა. ) გამოიყენებდა თვითნაბადი ოქროს გავრცელების წყალობით. არქეოლოგების ვარაუდით ოქროს სისტემური მოპოვება დაიწყეს ახლო აღმოსავლეთში, საიდანაც ოქროს სამკაულები მიეწოდებოდა დანარჩენ რეგიონებს, მათ შორის ეგვიპტეს. სწორედ ეგვიპტეში დედოფალი ზერისა და ერთერთი დედოფლის პუ-აბი ურის (შუმერების ცივილიზაცია) სამარხებშია ნაპოვნი ყველაზე ადრეული პირველი ოქროს სამკაულები, რომელიც თარიღდება III ათასწლეულით ჩ.წ.ა-მდე).
ფიზიკური თვისებები
სუფთა ოქრო - ყვითელი ფერის რბილი ლითონია. მოწითალო ელფერს ოქროს ზოგ ნაკეთობას (მაგალითად, მონეტებს) აძლევს სხვა ლითონების შერევა, კერძოდ კი სპილეძის. ოქროს თხელი ფირი შუქის გავლისას მწვანე ფერის ხდება. ოქროს გააჩნია ძალიან მაღალი თბოგამტარობა და დაბალი ელექტრო წინააღმდეგობა.
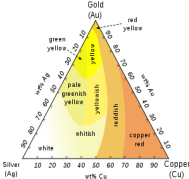
ოქრო, ვერცხლი, სპილენის შენადნობების ფერები
ოქრო ძალიან მძიმე ლითონია. სუფთა ოქროს სიმკვრივე ტოლია 19621 კგ/მ³ (სუფთა ოქროს ბურთი (სფერო) რომლის დიამეტრია 46 მმ იწონის - 1 კგ). ლიტრიანი ქილა, ავსებული ოქროს ქვიშით იწონის მიახლოებით 16 კგ. ეს თვისება გამოიყენება მოპოვებისას. ოქროს მოპოვების ყველაზე მარტივი ტექნოლოგიური პროცესია ქანების გამორეცხვა, რომლის დროსაც შესაძლებელია ოქროს საკმაოდ მაღალი ხარისხით გამოყოფა.
ოქრო ძალიან კარგი ჭედადი და წელვადი ლითონია. 1 გრამი ოქროს ნაჭერიდან შეიძლება მივიღოთ მავთული, რომლის სიგრძე იქნება 3 კილომეტრი ან დავამზადოთ კილიტა (ფოლგა), რომელიც 500-ჯერ თხელი იქნება, ვიდრე ადამიანის თმის ღერი (0.1 მკმ). სწორედ ასეთი თხელი კილიტა უშვებს სხივს, რომელიც მწვანე ფერს აძლევს მას. სუფთა ოქროს სირბილე ისეთი დიდია რომ, მისი გაჩხაპნა ფრჩხილითაც შეიძლება. ამიტომაც ოქრომჭედლობაში გამოიყენება მისი სპილენძთან ან ვერცხლთან შენადნობები. ასეთი შენადნობების შემადგენლობა განისაზღვრება სინჯით, რომელიც მიუთითებს 1000 წილ შენადნობში - ოქროს წონითი წილის რიცხვს. ქიმიურად სუფთა ოქროს სინჯია 999,9 — მას ასევე უწოდებენ «ბანკის» ოქროს, რადგან ასეთი ოქროსაგან ამზადებენ ზოდებს.
ქიმიური თვისებები
ოქრო ერთ-ერთი ყველაზე ინერტული ლითონია, რომელიც ლითონთა აქტივობის მწკრივში ყველა ლითონზე მარჯვნივ დგას, ნორმალური პირობების დროს ის არ ურთიერთქმედებს უმრავლეს მჟავეებთან და არ წარმოქმნის ოქსიდებს. ის განეკუთვნება კეთილშობილ ლითონებს
ოქროს ყველაზე მდგრადი დაჟანგვის ხარისხი შენაერთებში არის +3. ჟანგვის ამ ხარისხით ის ადვილად წარმოქმნის ერთ მუხტიან ანიონებთან (F−, Cl−. CN−) მდგრად ბრტყელ კვადრატულ კომლექსებს [AuX4]−.
ნაერთებში შედარებით მდგრადია ასევე +1 დაჟანგვის ხარისხით, რომელიც იძლევა კომპლექსებს [AuX2]−. დიდი ხნის განმავლობაში ითვლებოდა რომ +3 - ოქროს ყველაზე მაღალი დასაშვები დაჟანგვის ხარისხი იყო, მაგრამ, კრიპტონის დიფტორიდის გამოყენებით შესაძლებელი გახდა მიღებულიყო ნაერთი Au5+ (AuF5 ფთორიდი, [AuF6]− კომპლექსის მარილი). ოქროს (V) ნაერთები მხოლოდ ფთორთან არის სტაბილური და წარმოადგენენ უძლიერეს დამჟანგავებს.
ნივთიერებებში, სადაც ოქროს დაჟანგვის ხარისხი ფორმალურად არის +2, ნახევარი ოქრო როგორც წესი დაჟანგულია +1 ხარისხით, ხოლო ნახევარი ატარებს +3 ჟანგვით ხარისხს. მაგალითად, ოქროს (II) სულფატის AuSO4 სწორი იონური ფორმულა იქნება არა Au2+(SO4)2−, არამედ Au1+Au3+(SO4) 22−.
არსებობს ოქროს ნაერთები დაჟანგვის ხარისხით −1. მაგალითად CsAu (ცეზიუმის აურიდი) Na3Au (ნატრიუმის აურიდი). ეს შენაერთები იწოდებიან აურიდებად.
სუფთა მჟავეებიდან ოქრო იხსნება მხოლოდ ცხელ კონცენტრირებულ სელენის მჟავაში:
2 Au + 6 H2SeO4 → Au2(SeO4)3 + 3 H2SeO3 + 3 H2O
ოქრო შედარებით ადვილად რეაგირებს ჟანგბადთან და სხვა დამჟანგავებთან კომპლექს წარმომქმნელებთან. ციანიდების წყლის ხსნარებში ჟანგბადთან კონტაქტის პირობებში, ოქრო იხსნება და წარმოქმნის ციანოაურატებს:

220 კგ-იანი ოქროს ბრიკეტი ჯინგუაშის ოქროს მუზეუმი, ტაივანი
4 Au + 8 CN− + 2 H2O + O2 → 4 [Au(CN)2]− + 4 OH−
ციანოაურატები ადვილად აღდგებიან სუფთა ოქრომდე:
2 Na[Au(CN)2] + Zn → Na2[Zn(CN)4] + 2 Au
ქლორთან რეაქციის შემთხვევაში კომპლექს წარმოქმნის შესაძლებლობა მნიშვნელოვნად აადვილებს რეაქციის მიმდინარეობას: თუ კი მშრალ ქლორთან ოქრო რეაგირებს ~200 °C-ზე ოქროს (III) ქლორიდის წარმოქმნით, კონცენტრირებული მარილმჟავის და აზოტმჟავის (სამეფო არაყი) ხსნარებში ოქრო იხსნება ქლორაურატ-იონის წარმოქმნით ოთახის ტემპერატურის პირობებში:
2 Au + 3 Cl2 + 2 Cl− → 2 [AuCl4]−
ოქრო ადვილად რეაგირებს თხევად ბრომთან და მის წყლის და ორგანულ გამხსნელების ხსნარებთან AuBr3 წარმოქმნით.
ფთორთან ოქრო რეაგირებს 300−400 °C ტემპერატურის ინტერვალში, უფრო დაბალ ტემპერატურაზე რეაქცია არ მიდის, ხოლო უფრო მაღალ ტემპერატურაზე ოქროს ფთორიდები იშლებიან.
ოქრო ასევე იხსნება ვერცხლისწყალში და ფაქტიურად წარმოქმნის ადვილად დნობად შენადნობს (ამალგამას).

მსოფლიოში ყველაზე დიდი ოქროს ზოდი (250 კგ)
ტოის მუზეუმი, იაპონია
გავრცელება
ოქროს შემცველობა დედამიწის ქერქში ძალიან მცირეა და შეადგენს მხოლოდ 0.5-5 მკგ/კგ, თუმცა გარკვეულ ადგილებში თავმოყრილია ისეთი რაოდენობით, რომ მისი მოპოვება შესაძლებელი ხდება. ოქროს გარკვეული რაოდენობით წყალიც შეიცავს. 1 ლ ზღვის და მდინარის წყალს მოაქვს დაახლოებით 4×10−9 გ ოქრო, რაც შეესაბამება 4 კილოგრამ ოქროს 1 კუბურ კილომეტრ წყალში.
ოქროს მადნიანი საბადოები წარმოიქმნება უპირატესად გრანიტოიდების განვითარების რაიონებში.
ბუნებაში ცნობილია 15 ოქროს შემცველი მინერალი:
- თვითნაბადი ოქრო ვერცხლის, სპილენძის და სხვა მინარევით
- ელექტრუმი - Au და 25 - 45 % Ag
- პორპესიტი AuPd
- სპილენძიანი ოქრო, როდიუმიანი ოქრო, ირიდიუმიანი ოქრო, პლატინისტური ოქრო
- ბისმუტოაურიტი (Au, Bi)
- დანარჩენი მინერალები წარმოდგენილია ოქროს ტელურიდებით:
- კალავერიტი AuTe2
- კრენერიტი AuTe2
- სილვანიტი AuAgTe4
- პეტციტი Ag3AuTe2
- მუტმანიტი (Ag, Au)Te
- მონტბრეიიტი Au2Te3
- ნაგიაგიტი Pb5AuSbTe3S6.
ოქროსათვის დამახასიათებელია თვითნაბადი ფორმა. სხვა მის ფორმებს შორის აღნიშვნის ღირსია ელექტრუმი, ოქროსა და ვერცხლის შენადნობი, რომელსაც მომწვანო ელფერი დაჰკრავს და შედარებით ადვილად იშლება წყლით გადატანისას. ქანებში ოქრო ჩვეულებრივ გაბნეულია ატომარულ დონეზე. საბადოებში ის შედის სულფიდების და არსენიდების შემადგენლობაში.
განასხვავებენ ოქროს პირველად და კომპლექსურ მადნიან საბადოებს. პირველადი საბადოები წარმოადგენს ქვიშრობებს, სადაც ოქრო გვხვდება მადნეულიანი საბადოების დაშლის შედეგად მიღებული თვითნაბადი სახით. კომპლექსურ მადნიანი საბადოები კი მოიცავენ ოქროს სხვა თანამდევ კომპონენტთან ერთად.
მიღება
კაცობრიობის მთელი ისტორიის განმავლობაში მოპოვებულ იქნა დაახლოებით 140 ათასი ტონა ოქრო (ეს ოქრო ერთად რომ გადავადნოთ, მივიღებთ კუბს, რომლის გვერდის სიგრძე იქნება 19 მ).
ოქროს მოპოვების ლიდერები არიან:
- ჩინეთი (2007 წ. მოიპოვა 275 ტ, ხოლო 2008 წ. - 295 ტ)
- სამხრეთ აფრიკის რესპუბლიკა (252/250)
- აშშ (238/230)
- ავსტრალია (246/225)
- პერუ (170/175)
- რუსეთი (157/165)
- კანადა (101/100)
- ინდონეზია (118/90)
- უზბეკეთი (85/85)
- განა (84/84)
- პაპუა-ახალი გვინეა (65/65)
- ჩილე (42/42)
- მექსიკა (39/41)
- ბრაზილია (40/40)
ოქროს მოპოვებისას გამოიყენება მისი როგორც ქიმიური, ასევე ფიზიკური თვისებები. ქიმიური ინერტულობის გამო ბუნებაში თვითნაბადი სახით არსებობს. თანამედროვე ტექნოლოგიების განვითარების პირობებში უფრო პოპულარული ხდება მოპოვების ქიმიური ხერხები.

4.5 კგ–იანი ზოდი იქნა ნაპოვნი კალიფორნიაში
გამორეცხვა
გამორეცხვის მეთოდი ეფუძნება ოქროს მაღალ სიმკვრივეს, რის გამოც წყლის ჭავლში მინერალები, რომელთა სიმკვრივე ნაკლებია, ვიდრე ოქროსი (ასეთი კი დედამიწის ქერქის თითქმის ყველა მინერალია) გამოირეცხებიან და ლითონი კონცენტრირდება მძიმე ფრაქციაში, ქვიშაში, რომელიც შედგება მაღალი სიმკვრივის მქონე მინერალებისაგან. მცირე მოცულობით ოქროს მისაღებად შესაძლებელია ხელით გამორეცხვა. ეს მეთოდი უძველესი დროიდან გამოიყენებოდა. ამ მეთოდის ფართოდ გამოყენება კოლხეთის სამეფოშიც დადასტურებული და ასახულია ოქროს საწმისის ლეგენდაში, ბერძნები კოლხეთს ოქრომრავალ ქვეყანად მოიხსენიებენ და გამოსარეცხი ხონჩის მაგივრობას აქ ცხვრის ტყავი წევდა. მათ მდინარეებში აწყობდნენ და ოქროს ქვიშა ტყავის ბეწვში ილექებოდა. ეს მეთოდი და ხერხი ახლაც გამოიყენება პატარა ოქროს ქვიშრობი საბადოების შემთხვევაში. მაგრამ ის ძირითადად გამოიყენება - ოქროს, ალმასის და სხვა ძვირფასი ლითონების საბადოების ძიებისას . გამორეცხვის მეთოდი გამოიყენება მსხვილი ქვიშრობი საბადოების დამუშავებისას, მაგრამ ამ დროს გამოიყენება სპეციალური ტექნიკური საშუალებები: დრაგები და გამოსარეცხი დანადგარები. ბოლოს მიღებული მძიმე ქვიშა, ოქროს გარდა, შეიცავს სხვა მრავალ სხვა მკვრივ მინერალს, საიდანაც სუფთა ოქრო მიიღება, ქიმიური დამუშავების მაგ. ამალგაციის გზით.
გამორეცხვის მეთოდით მუშავდება ყველა ოქროს ქვიშრობი საბადოები, შეზღუდულად გამოიყენება ძირეულ საბადოებში. ამისათვის ქანებს ჯერ ამტვრევენ, აქუცმაცებენ და შემდეგ ხდება მათი გამორეცხვა.
ეს მეთოდი არ გამოიყენება ისეთი საბადოების დამუშავებისათვის, რომელიც ოქროს გაფანტული სახით მოიცვას, რადგან ოქროს მტვერი ადვილად მიყვება წყალს.
გამორეცხვის მეთოდი ძალიან იაფია რადგან არ საჭიროებს ძვირადღირებული ქარხნების მშენებლობას. ეკონომიკურად რენტაბელურია ქვიშრობების დამუშავება, რომლებშიც ოქროს შემცველობა არის 0.1 გ/ 1 კუბურ მეტრ დაქუცმაცებულ ქანებში.
2.png)
ოქროს მოპოვება 2005 წელს
ამალგაცია
ამალგამაციის მეთოდი დაფუძნებულია ვერცხლისწყლის უნარზე შექმნას შენადნობები - ამალგამები სხვადასხვა ლითონებთან, მათ შორის ოქროსთან.
ოქროს ამალგაციის გზით მიღებისას დანამულ და დაქუცმაცებულ ოქროს შემცველ ქანს ურევენ ვერცხლისწყალს და მიღებულ მასას ფქვავენ წისქვილში. მიიღება ოქროს ამალგამა, საიდანაც ოქროს გამოყოფენ გამორეცხვით. საბოლოოდ ვერცხლისწყალს აცილებდნენ შეგროვილი ამალგამიდან, რომელიც პროცესში უკან ბრუნდება. ამალგამაციის მეთოდი ცნობილია ჩვენი წელთაღრიცხვის I საუკუნიდან. მან ყველაზე დიდი გამოყენება ჰპოვა ესპანეთის ამერიკულ კოლონიებში XVI საუკუნის დასაწყისიდან, ასაც ხელი შეუწყო ესპანეთში არსებული ვერცხლისწყლის უდიდესი საბადოს ალმადენის აღმოჩენამ.
მოგვიანებით შემუშავდა გარე ამალგამაციის მეთოდი, როდესაც დაქუცმაცებული ოქროს შემცველი ქანების გამორეცხვისას უშვებენ გამამდიდრებელ სპილენძის ფურცლებით მოჭედილ და ვერცხლისწყლის თხელი ფენით დაფარულ რაბებში.
ამალგამაციის მეთოდი გამოიყენება მხოლოდ ისედ საბადოებში სადაც ოქროს მაღალი შემცველობაა. ეხლა ეს მეთოდი ძალიან იშვიათად გამოიყენება.
ციანიდური მეთოდი
ოქრო იხსნება ციანმჟავაში და მის მარილებში. მისმა ამ თვისებამ ჰპოვა გამოყენება ოქროს მოპოვების მთელ რიგ მეთოდებში, რომელსაც მადნის ციანირება ეწოდება.
_chloride_solution.jpg)
ოქროს (III) ქლორიდის წყალხსნარი
ციანიდური მეთოდი დაფუძნებულია ოქროს რეაქციაზე ციანიდებთან ჰაერის ჟანგბადის არსებობის პირობებში: დაქუცმაცებული ოქროს შემცველი ქანები მუშავდება განზავებული (0.3-0.03 %) ნატრიუმის ციანიდის ხსნარით, ოქრო წარმოქმნილი ნატრიუმის ციანოაურატის ხსნარიდან Na[Au(CN)2] გარს ერტყმის ან თუთიას მტვერი, ან სპეციალურ იონოცვალებად ფისებზე.
ციანიდური მეთოდი თავდაპირველად გამოიყენებოდა დიდ ქარხნებში, სადაც ქანები ქუცმაცდებიდა და ციანირება მიმდინარეობდა სპეციალურ საცავებში. მაგრამ ტექნოლოგიების განვითარებამ გამოიწვია ახალი მეთოდის გაჩენა - რომელიც შემდეგში მდგომარეობს: ამზადებენ წყალგაუმტარ მოედანს, მასზე ყრიან დაფქვილ მადანს და შემდეგ რწყავენ ციანიდების ხსნარებით, რომელიც, მადნის მთელ სისქეზე იჟონება და ხსნის ოქროს. ამის შემდეგ ის შედის სპეციალურ სორბციულ (შთანმთქმელ) კოლონებში, სადაც ოქრო მას გარს ერტყმის, ხოლო რეგენერირებული ხსნარი კვლავ უბრუნდება გროვას.
ციანიდური მეთოდი შეზღუდულია მადნის მინერალური შემადგენლობით. ის არ გამოიყენება, თუ მადანი დიდი რაოდენობით შეიცავს სულფიდებს ან არსენიდებს, რადგანაც ციანიდები ამ მინერალებთან რეაგირებენ. ამიტომაც ციანიდირებით მუშავდება მცირე სულფიდური მადნები ან მადნები დაჟანგვის ზონიდან, სადაც სულფიდები და არსენიდები დაჟანგულნი არიან ატმოსფერული ჟანგბადით.
სულფიდური მადნებიდან ოქროს ამოღებისათვის გამოიყენება რთული მრავალ საფეხურანი ტექნოლოგიები. საბადოდან მიღებულ ოქროს აქვს ბევრი მინარევი, ამიტომაც მიმდინარეობს მაღალი გაწმენდის სპეციალური პროცესები, რომელიც წარმოებს ოქროს აფინაჟის ქარხნებში.
გამოყენება
ოქრო წარმოადგენს მსოფლიო ფინანსური სისტემის უმნიშვნელოვანეს ელემენტს, რადგანაც ეს ლითონი არ განიცდის კოროზიას. გააჩნია ტექნიკური გამოყენების მრავალი სფერო, ხოლო მისი მარაგი არც ისე დიდია. ოქრო პრაქტიკულად არ დაკარგულა ისტორიული კატაკლიზმების პროცესებში, არამედ გროვდებოდა და მათი გადადნობა ხდებოდა. დღეისათვის მსოფლიო საბანკო ოქროს რეზერვები შეფასებულია 32 ათას ტონად.
ბევრი ერი ოქროს თავიდანვე იყენებდა როგორც ფულს. ოქროს მონეტა - ყველაზე კარგად შენახული უძველესი ძეგლია. მაგრამ როგორც მონოპოლური ფულადი საქონელი ის განმტკიცდა მხოლოდ XIX საუკუნეში. პირველი მსოფლიო ომის ბოლომდე ყველა მსოფლიო ვალუტა ეფუძნებოდა ოქროს სტანდარტს (1870 -1914 წწ პერიოდს უწოდებენ «ოქროს საუკუნეს»). ქაღალდის კუპიურა ამ დროს ასრულებდა ოქროს არსებობის მოწმობის როლს. ისინი თავისუფლად იცვლებოდა ოქროზე.
თავისი ქიმიური მდგრადობითა და მექანიკური სიმტკიცით ოქრო უთმობს პოზიციას უმეტეს პლატინოიდებს, მაგრამ შეუცვლელია როგორც ელექტრო კონტაქტი. ამიტომაც მიკროელექტრონიკაში ოქროს გამტარები და კონტაქტების ზედაპირის გალვანური დაფარვა, ჩამრთველები და სხვა გამოიყენება ფართოდ.
ოქროს რჩილი კარგად აკავშირებს სხვადასხვა ლითონის ზედაპირებს და გამოიყენება ლითონების მირჩილვისათვის. თხელი შუასადები, დამზადებული ოქროს რბილი შენადნობებისაგან, გამოიყენება ზეძლიერ ვაკუუმის ტექნიკაში.
ლითონთა მოოქროვება (ძველად - მხოლოდ ამალგამური მეთოდი, ეხლა კი - უპირატესად გალვანური მეთოდი) ფართოდ გამოიყენება როგორც კოროზიის საწინააღმდეგო დაცვის მეთოდი. მაგრამ არაკეთილშობილი ლითონების მოოქროვებას აქვს არსებითი ნაკლოვანებები (საფარის სირბილე, წერტილოვანი კოროზიის მაღალი პოტენციალი).
ოქრო დარეგისტრირებულია კვების მრეწველობაში როგორც საკვები დანამატი Е175.

ტუტანჰამონის ნიღაბი
ოქროს ტრადიციულ და ყველაზე მსხვილ მომხმარებელს წარმოადგენს საიუველირო მრეწველობა - ოქრომჭედლობა. საიუველირო ნაკეთობანი არ მზადდებიან სუფთა ოქროსაგან, არამედ იყენებენ ისეთ სხვა ლითონებთან შენადნობების სახით, რომლებიც მექანიკური სიმტკიცითა და მდგრადობით აღემატებიან ოქროს. ასეთ მეტალებს კი ძირითადად წარმოადგენს სპილენძი, ვერცხლი, ნიკელი, პალადიუმი, პლატინა, თუთია, კობალტი. აღსანიშნავია, რომ ეს მეტალები მეტაქნიკურ თვისებებთან ერთად ხშირად ოქროს ნამზადის ფერზეც არიან პასუხისმგებლები.
ოქროს მნიშვნელოვანი ნაწილი იხმარება სტომატოლოგიაში: სტომატოლოგიური გვირგვინები და კბილის პროთეზები მზადდებიან ოქროსა და ვერცხლის, ნიკელის, სპილენძის, პლატინის, თუთიის შენადნობების გამოყენებით. ასეთი შენადნობები უთავსებენ კოროზიულ მდგრადობას მაღალ მექანიკურ თვისებებს.
ოქროს ნაერთები შედის რამდენიმე სამედიცინო პრეპარატის შემადგენლობაში, რომელიც გამოიყენება მთელი რიგი დაავადებების სამკურნალოდ (ტუბერკულოზი, რევმატოიდული ართრიტი და ა.შ.).
რადიოაქტიული ოქრო გამოიყენება ავთვისებიანი სიმსივნეების სამკურნალოდ.
ბიოლოგიური როლი
ოქროს ზოგიერთი ნაერთი ტოქსიკურია. გროვდება თირკმლებში, ღვიძლში, ელენთაში და ჰიპოთალამუსში იწვევს მთელ რიგ დაავადებებს, მათ შორის დერმატიტებს, სტომატიტს და ტრომბოციტოპენიას. ოქროს ორგანული ნაერთები (პრეპარატები კრიზანოლი და აურანოფინი) გამოიყენება მედიცინაში აუტოიმუნური დაავადებების, კერძოდ კი რევმატოიდური ართრიტის სამკურნალოდ.
მასალა მომზადებულია www.wikipedia.com -ის მიხედვით



