მოლიბდენი
მოლიბდენი წარმოადგენს მე-6 ჯგუფის ქიმიურ ელემენტს. მისი სიმბოლოა Mo, ატომური ნომერია - 42. სახელი წარმოდგება ნეო–ლათინური Molybdaenum-ისგან, რომელიც დაფუძნებულია უძველეს ბერძნულ Molybdos-ზე. Molybdaenum ნიშნავს ტყვიას და ეს სახელი მიენიჭა საბადოს გამო, რომელიც შეცდომით მიიჩნიეს ტყვიის საბადოდ.
თავისუფალი სახით იგი წარმოადგენს ვერცხლისებრ მეტალს და აქვს ექვსჯერ უფრო მაღალი ლღობის ტემპერატურა, ვიდრე რომელიმე მეტალს. იგი ადვილად წარმოქმნის მაგარ, სტაბილურ კარბიდებს და ამის გამო ხშირად გამოიყენება გამძლე ფოლადის შენადნობებში.
მოლიბდენი ბუნებაში თავისუფალი სახით არ მოიპოვება, თუმცა მინერალებში გვხვდება სხვადასხვა დაჟანგულობის რიცხვით. ინდუსტრიაში მოლიბდენის შენაერთები გამოიყენება მაღალი წნევისა და მაღალი ტემპერატურის პირობებში, როგორიცაა პიგმენტები და კატალიზატორი.
მოლიბდენის მინერალები დიდი ხანია ცნობილია, მაგრამ როგორც ელემენტი აღმოჩენილი იქნა 1778 წელს კ.შეელეს მიერ. მეტალი პირველად 1781 წელს პ. ჰელმმა გამოყო.
მოლიბდენის ნაერთების უმეტესობა წყალში მცირედ ხსნადია, თუმცა მოლიბდენ–შემცველ მინერალებს ჟანგბადთან და წყალბადთან ურთიერთქმედების დროს შეუძლია წარმოქმნას წყალში ხსნადი MnO42- იონი.
ისტორია
მოლიბდენიტი – ძირითადი საბადო, რომლისგანაც ამჟამად ხდება მოლიბდენის ექსტრაქცია, პირველ ეტაპზე მიჩნეული იყო გრაფიტის საბადოდ. გრაფიტის გამოყოფის შემდეგ რჩებოდა მეტალი, რომელიც მიეწერა ტყვიას. ამიტომ დაერქვა ამ საბადოს „molybdena”, ძველი ბერძნული სიტყვიდან „molybdos” (ნიშნავს ტყვიას).
1754 წელს ბ. ოვისთმა გამოცადა მოლიბდენიტი და განსაზღვრა, რომ ის არ შეიცავდა ტყვიას (არ იყო გალენიტი).
1778 წელს შვედმა ქიმიკოსმა კ .შეელემ დაადგინა, რომ „molybdena” არ იყო არც გრაფიტი და არც ტყვია. კვლევის შედეგები მან ქიმიკოსთა საზოგადოებას მიაწოდა და აუწყა, რომ საბადო მოიცავდა მანამდე უცნობ ელემენტს - მოლიბდენს. მოგვიანებით, 1781 წელს პ. ჯელმა წარმატებით გამოიყო მოლიბდენი თავისუფალი სახით.
გავრცელება
მოლიბდენის და მისი ნაერთების უდიდესი მსოფლიო მწარმოებლებია: აშშ, ჩილე, პერუ და კანადა. 1885 -1995 წლებში მოლიბდენის მოპოვება წარმოებდა ნორვეგიაშიც.
მოლიბდენი გვხვდება მინერალებში – ვულფენიტი (PbMoO4) და პოველიტი (CaMoO4). მოლიბდენის ძირითადი კომერციული წყაროა მოლიბდენიტი (MoS2). იგი ხშირად თანაური პროდუქტის სახით გვხვდება სპილენძისა და ვოლფრამის საბადოებში.
მოლიბდენი გავრცელების მიხედვით წარმოადგენს 54-ე ელემენტს დედამიწის ქერქში და 25–ე ელემენტს. იგი 42-ე ელემენტია გავრცელების მიხედვით მთელ სამყაროში.

მოლიდბენიტი კვარცზე
იზოტოპები
ცნობილია მოლიბდენის 32 იზოტოპი ატომური მასით 83-დან 117-მდე და ასევე ოთხი მეტასტაბილური იზოტოპი. შვიდი იზოტოპი გავრცელებულია შენადნობში, რომელთა ატომური მასაა 92, 94, 95, 96, 97, 98 და 100. ამ იზოტოპებიდან არასტაბილურია მხოლოდ მოლიბდენ-92 და მოლიბდენ-100. მოლიბდენის ყველა არამდგრადი იზოტოპი იშლება ნიობიუმის, ტექნეციუმის და რუთენიუმის იზოტოპებად.
მოლიბდენ -98 ყველაზე გავრცელებული იზოტოპია (24.14%). მოლიბდენ-100–ის ნახევარდაშლის პერიოდია დაახლოებით 1019 წელი და განიცდის bb-დაშლას რუთენიუმ–100-მდე. მოლიბდენის ყველა იზოტოპების მასით 111-დან 117-მდე ნახევრდაშლის პერიოდია დაახლოებით 150 ნანოწმ.
ფიზიკური თვისებები
თავისუფალი სახით მოლიბდენი წარმოადგენს მოვერცხლისფრო მეტალს, რომლის სიმაგრე უდრის 5.5 (მოხის შკალით). მისი ლღობის ტემპერატურაა 2623 °C. იმ ელემენტებიდან, რომლებიც გავრცელებულია ბუნებაში, მხოლოდ ტიტანს, ოსმიუმს, რენიუმს, ვოლფრამს და ნახშირბადს აქვს უფრო მაღალი ლღობის წერტილი. მოლიბდენი იწვის მხოლოდ 600°C-ზე. მოლიბდენს კომერციულად გამოყენებულ მეტალებს შორის გააჩნია ყველაზე დაბალი თერმული გაფართოების კოეფიციენტები.
ქიმიური თვისებები
მოლიბდენი ამჟღავნებს რამდენიმე დაჟანგულობის რიცხვს. მდგრადი ნაერთებია +4 და +6 ჟანგვითი რიცხვით.
მოლიბდენი გარდამავალი მეტალია, რომლის ელექტროუარყოფითობა პოლინგის შკალის მიხედვით ტოლია 1.8. იგი არ ურთიერთქმედებს ჟანგბადთან და წყალბადთან ოთახის ტემპერატურაზე. მაღალ ტემპერატურაზე წარმოიქმნება მოლიბდენის ტრიოქსიდი.
2 Mo + 3 O2 → 2 MoO3
მოლიბდენის და მისი ნაერთების თვისებები უფრო მეტ მსგავსებას ამჟღავნებენ ვოლფრამთან, ვიდრე ქრომთან. ამის მაგალითს წარმოადგენს მოლიბდენ(III) და ვოლფრამ (III) ნაერთების არასტაბილურობა ქრომ(III) ნაერთებთან შედარებით.
უმაღლესი დაჟანგულობის რიცხვი მოლიბდენ (VI) გვხვდება ოქსიდში MoO3, ხოლო მინიმალური - მოლიბდენის დისულფიდში MoS2.
მოლიბდენ (VI) ოქსიდი იხსნება ძლიერ ტუტეებში და წარმოქმნის მოლიბდატებს MoO42-. მოლიბდატები ქრომატებთან შედარებით სუსტი დამჟანგველებია, მაგრამ ისინი ამჟღავნებენ ტენდენციას წარმოქმნან ოქსიანიონის კომპლექსები [Mo7O24]6- და [Mo8O26]4- დაბალი pH–ის დროს. პოლიმოლიბდატები შეიძლება გაერთიანდეს სხვა იონებთან და წარმოქმნას პოლიქრომეტალები.
მუქი ლურჯი შეფერილობის ფოსფორშემცველი ჰეტეროპოლიმოლიბდატი P[Mo12O40]3- გამოიყენება ფოსფორის სპექტროსკოპული აღმოჩენისთვის.
მოლიბდენი დაჟანგულობის რიცხვის ფართო სპექტრს ამჟღავნებს სხვადასხვა მოლიბდენ–ქლორიდებში.
- მოლიბდენ (II) ქლორიდი, MoCl2(მყარი, ყვითელი)
- მოლიბდენ (III) ქლორიდი MoCl3(მყარი, მუქი წითელი)
- მოლიბდენ (IV) ქლორიდი MoCl4(მყარი, შავი)
- მოლიბდენ (V) ქლორიდი MoCl5(მყარი, მუქი მწვანე)
- მოლიბდენ(VI) ქლორიდი MoCl6(მყარი, ყავისფერი)
ქრომის და სხვა გარდამავალი მეტალების მსგავსად, მოლიბდენს შეუძლია წარმოქმნას ოთხმაგი ბმები(მაგ. ნაერთში Mo2(Cu3COO)4). ეს ნაერთი შეიძლება გარდაიქმნას Mo2Cl84-, რომელსაც ასევე არსებობს ოთხმაგი ბმები.
დაჟანგულობის რიცხვი 0 გვხვდება მოლიბდენ ჰექსაკარბონილში Mo(CO)6.
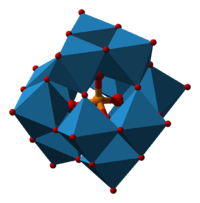
ფოსფომოლიბდატის ანიონის კეგინის სტრუქტურა (P[Mo12O40]3−)
მიღება
მოლიბდენიტს თავდაპირველად აცხელებენ 700°C-ზე და მიღებულ სულფიდს ჟანგავენ ჰაერზე, რის შედეგადაც მიიღება მოლიბდენ(VI) ოქსიდი:
2 MoS2 + 7 O2 → 2 MoO3 + 4 SO2
მოლიბდენ (VI) ოქსიდი, ამიაკთან ურთიერთქმედებით იძლევა წყალში ხსნად მოლიბდატს:
MoO3 + 2 MN4OH → (NH4)2(MoO4) + H2O
მოლიბდენიტი სპილენძის მონარევებით ამიაკში ნაკლებ ხსნადია. ხსნარიდან მისი გამოყოფა შესაძლებელია გოგირდწყალბადით გამოლექვით.
სუფთა მოლიბდენი მიიღება ოქსიდის წყალბადით აღდგენით.
მოლიბდენს ამატებენ რკინას და მიიღება ფერომოლიბდენი, რომელიც შეიცავს 60% მოლიბდენს.
გამოყენება

MoSi2-ის გამახურებელი ელემენტი
მოლიბდენი მდგრადი მეტალია. იგი საკმაოდ დრეკადია ექსტრემალურ ტემპერატურაზეც მნიშვნელოვანი დანაკარგების გარეშე, რაც შესაძლებლობას იძლევა გამოვიყენოთ თვითმფრინავების ნაწილების ელექტრული კონტაქტების, ძრავის დეტალებისა და ბოჭკოების წარმოებაში.
მაღალი მდგრადობის ფოლადის შენადნობი (მაგალითად 41xx ფოლადი), შეიცავს 0.25%-დან 8%-მდე მოლიბდენს. მიუხედავად მოლიბდენის ასეთი მცირე ნაწილისა, ყოველწლიურად 43 000 ტონაზე მეტი მოლიბდენი გამოიყენება, როგორც მალეგირებელი აგენტი ნაკლებად ჭიმვად ფოლადში, თუჯისა და სხვა მაღალტემპერატურულ შენადნობებში.
მოლიბდენი ფოლადის შენადნობებში გამოიყენება მაღალი კოროზიამედეგობისა და შედუღების უნარის გაუმჯობესების მიზნით.
დაბალი სიმკვრივისა და სტაბილური ფასების გამო მოლიბდენი ზოგჯერ გამოიყენება ვოლფრამის ნაცვლად. ამის მაგალითია „M“ სერიის ადვილად საჭრელი ფოლადები (M2, M4 და M42), რომელიც ანაცვლებს ვოლფრამის შემცველ „T” სერიის ფოლადებს.
მოლიბდენის სხვა შენადნობები, რომლებიც არ შეიცავენ რკინას, აქვთ შეზღუდული გამოყენება. ზოგჯერ კოროზიამედეგი მოლიბდენი და მოლიბდენ/ვოლფრამის (70%/30%) გამოიყენება თუთიის ნაცვლად (წყალსაქაჩ ტუმბოებში, ძრავებში, სხვადასხვა მილგაყვანილობაში).
მეტალური მოლიბდენი მნივშნელოვანი კონსტრუქციული მასალაა ელექტროგანათებელი ნათურებისა და ელექტროვაკუუმ დანადგარების ნაწილების წარმოებაში (რადიონათურები, გენერატორის ნათურები, რენტგენის მილები და სხვა.), სადაც მოლიბდენის მავთულისაგან, ამზადებენ სხვადასხვა დეტალებს: როგორიცაა ანოდები, კათოდები, ძაფების დამჭერი და სხვა.
ბოლო ხანებში მოლიბდენი გამოიყენება იმ შემთხვევაში, როცა აუცილებელია მაღალ ტემპერატურაზე გამძლეობის შენარჩუნება. მაგალითად, მაღალ ტემპერატურაზე ჟანგვისაგან თავის არიდების მიზნით იყენებენ მეტალს დაფარვას მოლიბდენის სილიციდით.
ტექნიკაში MoS2 იყენებენ, როგორც საცხის დანამატ მასალას. ნატრიუმის მოლიბდატი გამოიყენება საღებრების და ლაქების წარმოებაში. ტყვისს მოლიბდატი (ვულფენიტი) ილექება ტყვიის ქრომატთან და ტყვიის სულფატთან ერთად მოწითალო–ნარინჯისფერი პიგმენტის სახით გამოიყენება კერამიკასა და პლასტმასების წარმოებაში.
მოლიბდენ ტრიოქსიდი გამოიყენება ემალსა და მეტალს შორის, როგორც ადგეზიური ნაერთი.
მოლიბდენის ფხვნილი გამოიყენება სასუქად ზოგიერთი მცენარეებისთვის (მაგალითად ყვავილოვანი კომბოსტოსათვის).
მოლიბდენ-99 გამოიყენება არაერთ სამედიცინო პროცედურებში. ამონიუმის ჰეპტამოლიბდატი გამოიყენება ბიოლოგიურ პროცედურებში (ფერად რეაქციებში).
მოლიბდენი აგრეთვე გამოიყენება NO, NO2, NOx ანალიზატორებში, მცენარეების დაბინძურების კონტროლისათვის. 350°C-ზე მოლიბდენი, როგორც კატალიზატორი ურთიერთქმედებს NO2/NO –თან და წარმოქმნის მხოლოდ NO–ს მოლეკულებს, რომელიც ვლინდება ინფრაწითელი სხივებით.
ბიოლოგიური როლი
ცოცხალ ორგანიზმებში მოლიბდენი გვხვდება ჰეტეროატომის სახით ენზიმის ცენტრში. ზოგიერთ ბაქტერიაში აზოტის ფიქსაციის დროს, ენიზმი ნიტროგენაზა შეიცავს მოლიბდენს აქტიურ ცენტრში (ზოგჯერ მოლიბდენი ჩანაცვლებულია რკინით ან ვანადიუმით).
ადამიანის ორგანიზმი შეიცავს 0.07 მგ მოლიბდენს (წონითი წილი ყოველ კილოგრამზე). იგი დიდი რაოდენობით გვხვდება ღვიძლში და თირკმელში, მცირე რაოდენობითაა ხერხემალში. მოლიბდენი ასევე გვხვდება ადამიანის კბილის ემალში და ხელს უშლის კბილის დაშლას.
ღორის, ბატკნის და ძროხის ღვიძლი, თითოეული შეიცავს დაახლოებით მოლიბდენის 1.5 მნ. სხვა მნიშვნელოვანი დიეტური საკვები, როგორიცაა მწვანე პარკოსანი მცენარეები ოსპა, კიტრი, პურის მარცვალი და სხვა. მცირე რაოდენობით ასევე შეიცავს მოლიბდენს.
მოლიბდენის დღიური საშუალო რაოდენობა 0.12–დან 0.24მგ–მდეა. ვირთხებზე ექსპერიმენტმა უჩვენა, რომ საშუალო ლეტარული დოზა (LD50), დაბალია 180 მგ/კგ.
ზოგიერთ კვლევაში ნაჩვენებია, რომ ადამიანებში მოლიბდენის მიღების რაოდენობა თუ აღემატება 10 მგ/დღეში, მას შეუძლია გამოიწვიოს დიარეა, ზრდის შენელება, წონაში კლება და ასევე პოდაგრა. მოლიბდენი გავლენას ახდენს ფილტვებზე, თირკმელებზე და ღვიძლზე.
ნატრიუმის მოლიბდატი წარმოადგენს მოლიბდენის ინჰიბიტორს. დიეტური ვოლფრამი აღადგენს მოლიბდენის კონცენტრაციას ქსოვილებში.
მოლიბდენის მტვერი და ორთქლი ტოქსიკურია განსაკუთრებით, თუ მისი შეწოვის დროს მოლიბდენის მცირე რაოდენობამ შეიძლება გამოიწვიოს თვალების და კანის გაღიზიანება. მოლიბდენის ოქსიდების 60–დან 600 მგ/გ3 რაოდენობასთან ხშირმა შეხებამ შეიძლება გამოიწვიოს დაღლილობა, თავის ტკივილი და სახსრების ტკივილი.
მასალა მომზადებულია www.wikipedia.com -ის მიხედვით



