| წინა ელემენტი |
|
შემდეგი ელემენტი |
სახე

მოვერცხლისფრო-ნაცრისფერი
ძირითადი თვისებები
| დასახელება, სიმბოლო, ნომერი |
თუთია, Zn, 30 |
| წარმოთქმა |
|
| ელემენტის კატეგორია |
გარდამავალი მეტალი |
| ჯგუფი, პერიოდი, ბლოკი |
12, 4, d |
| ატომური მასა |
65.38(4) გ მოლი-1 |
| ელექტრონული კონფიგურაცია |
[Ar] 3d10 4s2 |
| ელექტრონები ორბიტალებზე |
2, 8, 18, 2 |
ფიზიკური თვისებები
| აგრეგატული მდგომარეობა |
მყარი |
| სიმკვრივე |
7.14 გ სმ-3 |
| სიმკვრივე თხევად მგდომარეობაში (ლღობის ტემპერატურაზე) |
6.57 გ სმ-3 |
| ლღობის ტემპერატურა |
692.68 K, 419.53˚C |
| დუღილის ტემპერატურა |
1180 K, 907 ˚C, 1665 ˚F |
| კრიტიკული წერტილი |
|
| დნობის სითბო |
7.32 კჯ მოლი-1 |
| აორთქლების სითბო |
123.6 კჯ მოლი-1 |
| სპეციალური სითბოტევადობა |
(25 ˚C) |
| ორთლის წნევა | ||||||||||||||
|
ატომური თვისებები
| ჟანგვითი რიცხვები |
+2, +1, 0 |
| ელექტროუარყოფითობა |
1.65 (პოლინგის შკალა) |
| იონიზაციის ენერგიები |
I: 906.4 კჯმოლი-1 |
| ატომური რადიუსი |
134 pm |
| კოვანელტური რადიუსი |
122±4 pm |
| ვან დერ ვაალსის რადიუსი |
139 pm |
სხვადასხვა
| კრისტალური სტრუქტურა |
ჰექსაგონალური |
| მაგნიტური მოწესრიგებულობა |
დიამაგნიტური |
| კუთრი ელექტრული წინაღობა |
(20˚C) 59.0ნΏ მ |
| სითბოგამტარობა |
(300 K) 116 ვტმ-1K-1 |
| სითბოგადაცემა |
(25˚C) 30.2 µm m-1K-1 |
| ბგერის სიჩქარე |
(20˚C) 3850 მ/წმ |
| იუნგის მოდული |
108 გპა |
| შერის მოდული |
43 გპა |
| ბულკის მოდული |
70 გპა |
| სიმტკიცე მოსის მიხედვით |
2.5 |
| CAS-ის რეფისტრაციის ნომერი |
7440-66-6 |
მდგრადი იზოტოპები
| იზოტოპი | NA | ნახევარ-სიცოცხლე | DM | DE(MeV) | DP |
| 64Zn | 48.6% | 64Zn მდგრადია 34 ნეიტრონით | |||
| 65Zn | სინთ. | 243.8 დღე | ε | 1.3519 | 65Cu |
| γ | 1.1155 | - | |||
| 66Zn | 27.9% | 66Zn მდგრადია 36 ნეიტრონით | |||
| 67Zn | 4.1% | 67Zn მდგრადია 37 ნეიტრონით | |||
| 68Zn | 18.8% | 68Zn მდგრადია 38 ნეიტრონით | |||
| 70Zn | 0.6% | 70Zn მდგრადია 40 ნეიტრონით | |||
| 72Zn | სინთ. | 46.5 სთ | β- | 0.458 | 72Ga |
თუთია
თუთია – მენდელეევის ქიმიურ ელემენტთა პერიოდული სისტემის მეორე ჯგუფის, მეოთხე პერიოდის ელემენტი, ატომური ნომერია 30. აღინიშნება სიმბოლოთი Zn (ლათ. Zincum). მარტივი ნივთიერება თუთია (CAS - ნომერი: 7440-66-6)ნორმალურ პირობებში - წარმოადგენს მყიფე გარდამავალ მეტალს, მოცისფრო-მოთეთრო ფერის ლითონს (ჰაერზე ფერმკრთალდება, იფარება თუთიის ოქსიდის თხელი ფენით).
ისტორია
თუთიის სპილენძთან შენადნობი - ლატუნი - ცნობილი იყო ჯერ კიდევ ძველ საბერძნეთში, ძველ ეგვიპტეში, ინდოეთში (VII საუკუნე), ჩინეთში (XI საუკუნე). ძალიან დიდი ხნის განმავლობაში ვერ ხერხდებოდა შუფტა თუთიის გამოყოფა. 1746 წელს ა. ს. მარგგრაფმა შეიმუშავა სუფთა თუთიის მიღების მეთოდი, მისი ოქსიდების ნარევის შეცხობით ნახშირთან უჰაერო არეში, ცეცხლგამძლე თიხის რეტორტებში, მაცივრებში თუთიის ორთქლის შემდგომი კონდენსაციით. სამრეწველო მაშტაბით თუთიის გამოდნობა დაიწყო XVII საუკუნეში.
დასახელების წარმოშობა
სიტყვა ”თუთია” პირველად გვხვდება პარაცელსის შრომებში, რომელმაც დაასახელა ეს მეტალი ”zincum” ან ”zinken” წიგნში Liber Mineralium II. ეს სიტყვა ალბათ წარმოშობილია გერმანულიდან ”Zinke”, რაც ნიშნავს ”კბილს” (მეტალური თუთიიის კრისტალები ნემსისებურია).
ბუნებაში არსებობა

შპარელიტი (ZnS)
შედარებით გავრცელებულია თუთიის მინერალი - სფალერიტი ან თუთიის მატყუარა. მინერალის ძირიტადი კომპონენტია - თუთიის სულფიდი ZnS, ხოლო სხვადასხვა მინარევები ანიჭებენ მას ყველა შესაძლო ფერს. როგორც ჩანს ამის გამო ამ მინერალს უწოდებენ მატყუარას. თუთიის მატყუარას თვლიან პირველად მინერალად, რომლისგანაც წარმოიქმნა ელემენტ თუთიის სხვა მინერალები: სმიტსონიტი ZnCO3, ცინკიტი ZnO, კალამინი 2ZnO • SiO2 • Н2O.
წარმოშობა
თუთიის საბადოები ცნობილი ავსტრალიაში, ბოლივიაში.
მიღება
თუთია ბუნებაში, როგორც თვითნაბადი მეტალი არ გვხვდება. თუთიას მოიპოვებენ პოლიმეტალური საბადოებიდან, რომელიც შეიცავს 1-4% Zn-იას სულფიდის სახით, ასევე Cu, Pb, Ag, Au, Cd, Bi. მადნის გამდიდრება ხდება სელექციური ფლოტაციით და ღებულობენ თუთიის კონცენტრატებს (50-60% Zn) და ამავდროულად ტყვიის, სპილენძის და ზოგჯერ პირიტულ კონცენტრატებს. მდუღარე შრის ღუმელებში გამოწვავენ თუთიის კონცენტრატებს, თუთიის სულფიდი გადაჰყავთ თუთიის ოქსიდში ZnO. ამ დროს წარმოქმნილი გოგირდოვანი აირი ხმარდება გოგირდმჟავას წარმოებას. სუფთა თუთიას ოქსიდიდან ღებულობენ ორი მეთოდით. პირომეტალურგიული (დისტილაციური) მეთოდით, რომელიც ცნობილია დიდი ხანია, გამომწვარი კონცენტრატი ექვემდებარება შეცხობას მარცვლოვანობისა და აირგამტარობის მისანიჭებლად, შემდეგ მას აღადგენენ ნახშირით ან კოქსით 1200-1300 °С ტემპერატურაზე.
ZnO + С = Zn + CO
ძირითადი მეთოდი თუთიის მიღებისა - ელექტროლიტური (ჰიდრომეტალურგიული). გამომწვარ კონცენტრატებს ამუშავებენ გოგირდმჟავათი, მიღებულ სულფატურ ხსნარს ასუფთავებენ მინარევებისაგან (თუთიის მტვერის გამოლექვით) და ექვემდებარება ელექტროლიზს აბაზანაში. თუთია ილექება ალუმინის კათოდზე, რომლისგანაც მას ყოველდღე ასუფთავებენ და ალღობენ ინდუქციურ ღუმელებში. ჩვეულებრივ ელექტროლიტური თუთიის სისუფთავე 99.95%-ია. წარმოების ნარჩენებიდან ღებულობენ თუთიის აჯასპს, Pb, Cu, Cd, Au, Ag; ზოგჯერ ასევე In, Ga, Ge, Tl.
ფიზიკური თვისებები
თუთია სუფთა სახით - საკმაოდ პლასტიური მოვერცხლისფო-თეთრი მეტალია. ახასიათებს ჰექსაგონალური მესერი პარამეტრებით а = 0.26649 ნმ, с = 0.49468 ნმ. ოთახის ტემპერატურაზე მყიფეა, ფირფიტის მოღუნვისას ისმის კრისტალების დაბზარვის ხმა (ჩვეულებრივ ძლიერია, ვიდრე ”კალას ყვირილი”) 100-150 °C-ზე თუთია პლასტიურია. მინარევები, თუნდაც უმნიშვნელო, მკვეთრად ზრდიან თუთიის სიმყიფეს.
ქიმიური თვისებები

თუთიის აცეტატი
ტიპიური ამფოტერული მეტალი. სტანდარტული ელექტროდული პოტენციალი - 0.76ვ, სტანდარტული პოტენციალის რიგში განლაგებულია რკინამდე.
ჰაერში თუთია იფარება თუთიის ოქსიდის ZnO თხელი ფენით. ძლიერი გაცხელებისას იწვის და წარმოქმნის ამფოტერულ თეთრ ოქსიდს ZnO.
2Zn + O2 = 2ZnO
თუთიის ოქსიდი უერთიერთქმედებს, როგორც მჟავებთან:
ZnO + 2HNO3 = Zn(NO3)2 + H2O
ისე ტუტესთან
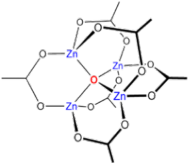
ფუძე თუთიის აცეტატი
ZnO + 2NaOH = Na2ZnO2 + Н2О
ჩვეულებრივი სისუფთავის თუთია აქტუურად ურთიერთქმედებს მჟავათა ხსნარებთან:
Zn + 2HCl = ZnCl2 + H2↑
Zn + H2SO4(განზ.) = ZnSO4 + H2↑
ასევე ტუტის ხსნარებთან და წარმოქმნის ჰიდროქსოცინკატებს:
Zn + 2NaOH + 2H2O = Na2[Zn(OH)4] + H2↑
მჟავასა და ტუტის ხსნარებთან ძალიან სუფთა თუთია არ ურთიერთქმედებს. ურთიერთქმედება იწყება რამოდენიმე წვეთი სპილენძის სულფატის CuSO4 დამატების შემდეგ.
გაცხელებით თუთია ურთიერთქმედებს ჰალოგენებტან და წარმოქმნის ჰალოგენიდებს ZnHal2. ფოსფორთან თუთია წარმოქმნის ფოსფიდებს Zn3P2 და ZnP2. გოგირდთან და მის ანალოგებთან - სელენთან და ტელურთან - სხვადასხვა ჰალკოგენიდებს ZnS, ZnSe, ZnSe2 და ZnTe. თუთიის სულფიდი გამოიყენება დროებითი მოქმედების ლუმინოფორების და ასევე სხვადასხვა სახის ლუმინესცენტების სინთეზისათვის, ZnS-სა და CdS-ის ნარევის ბაზაზე. ლუმინოფორები თუთიისა და კადმიუმის სულფიდის ბაზაზე, ასევე გამოიყენება ელექტრონულ წარმოებაში მანათობელი ელასტიური (მოქნილი) პანელებისა და ეკრანების დასამზადებლად ელექტროლუმინოფორების სახით და მოკლე ხანგრძლივობის გამონათების შემადგენლობების შესაქმნელად.

თუთიის ქლორიდი
წყალბადტთან, აზოტთან, ნახშირბადთან, სილიციუმთან და ბორთან თუთია პირდაპირ არ რეაგირებს. თუთიის ნიტრიდს Zn3N2 ღებულობენ თუთიის ამიაკთან ურთიერთქმედებით 550 - 600 °C ტემპერატურაზე.
წყალხსნარებში თუთიის იონები Zn2+ წარმოქმნიან აკვაკომპლექსებს [Zn(H2O)4]2+ და [Zn(H2O)6]2+.
გამოყენება
- მოთუთიება - 45-60%
- მედიცინაში (თუთიის ოქსიდი როგორც ანტისეპტიკი) – 10%
- შენადნობების წარმოება - 10%
- რეზინის საბურავების წარმოება - 10%
- ზეთოვანი საღებავები - 10%
სუფთა მეტალური თუთია გამოიყენება ძვირფასი ლითონების აღსადგენად, რომელიც მოიპოვება მიწისქვეშა გამოტუტვით (ოქრო, ვერცხლი). გარდა ამისა, თუთია გამოიყენება ვერცხლის, ოქროს (და სხვა მეტალების) ამოსაღებად შავი ტყვიიდან თუთიის ინტერმეტალიდების სახით ვერცხლთან და ოქროსთან (ე. წ. ”ვერცხლის ქაფი, ქერქი”), რომელიც შემდგომ ექვემდებარება ჩვეულებრივ აფინაჟის (( ფრანგ. affinage < affiner „გაწმენდა“, მაღალი სიწმინდის კეთილშობილი ლითონების მიღების პროცესი) მეთოდით დამუშავებას.
ფოლადისა და რკინის ნაკეთობების ატმოსფერული კოროზიისაგან დასაცავად მიმართავენ თუთიით დაფარვას სილაჭავლური გზით გაწმენდილ რკინის ზედაპირს ათავსებენ სპეციალურ ჭურჭელში და ახურებენ 440°C-მდე თუთიის მტვერთან ერთად. ამ ხერხით მიიღება რკინა-თუთიის დიფუზური შრე. რაც უფრო მაღალია ტემპერატურა, მით მეტია შეხების ხანგრძლივობა. თუთიის საფარის სისქე 0.05-0.06მმ-ია, რაც საკმარისია ნაკეთობის დასაცავად. რკინა არ დაიჟანგება მანამ, სანამ მის ზედაპირზე იქნება თუთია. თუთია რკინაზე უფრო უარყოფითი პოტენციალის მქონეა.
ელექტროქიმიური დაცვა
ეს მეთოდი შემუშავებულ იქნა რუსი მეცნიერის, იაკობის მიერ. ელექტროქიმიური დაცვა იხმარება ძირითადად ნიადაგში მოხეტიალე დენების ან ელექტროლიტების მოქმედებისაგან დასაცავად. სხვადასხვა ტიპის ნიადაგები სხვადასხვანაირად მოქმედებენ ამ პროცესზე. მაგ. თიხიანი ნიადაგები, რომელთაც ტუტე რეაქცია აქვთ, რკინის ნაკეთობებს კარგად ინახავენ. შესწავლილია, რომ მიწისქვეშა მილებზე ყველაზე ძლიერ კოროზიას ტორფიანი, წითელი და ცისფერი თიხიანი ნიადაგები ახდენენ. ქვიშიანი და ხრეშიანი ნიადაგები ყველაზე უვნებელი აღმოჩნდა. ამ მილებზე ძლიერ კოროზიას იწვევენ აგრეთვე მოხეტიალე დენების არხები. მოხეტიალე დენები ლითონს იმ ადგილებში აზიანებენ, სადაც ლითონებიდან დენი გარემო არეში გადადის (ანოდურ ზონაში) ხოლო იმ ადგილებში, სადაც ლითონში დენი შედის (კათოდური ზონა) ლითონი არ იშლება. აღმოჩნდა,რომ მოხეტიალე დენები ყველაზე მეტად არსებობენ ტორფიან, წითელ და ცისფერ თიხიან ნიადაგებში და ამიტომ აუცილებელია მიწისქვეშა წყალგაყვანილობის ელექტრონული დაცვა. მისი არსი შემდეგშია:
ელექტროლიტში დენის გატარებისას, კათოდზე განიმუხტება კატიონები. ე. ი. გამოილექება ლითონი. თუ ელექტროლიტი შეიცავს ZnSO4 და ანოდად გამოიყენებენ თუთიის ღეროს, ელექტროლიზის დროს კათოდზე განიმუხტება თუთიის იონები.
Zn2+ + 2e = Zn
ხოლო ანოდზე წავა შებრუნებული პროცესი. თუთიის ელექტროდი იწყებს გახსნას
Zn = Zn2+ + 2e
რის გამოც სხნარში Zn2+ იონების კონცენტრაცია მუდმივი იქნება. ასეთივე ხერხით ხდება მონიკელება, მოქრომვა და სხვ. საერთოდ ელექტროქიმიური დაფარვის გზით მიღებული საფარი უფრო სუფთა და ლამაზია.
ასევე გამოიყენება, მასალის სახით უარყოფითი ელექტროდისათვის დენის ქიმიური წყაროში, ანუ ბატარეებში და აკუმულატორებში. მაგალითად, მაგნიუმ-თუთიის ელემენტი, ვერცხლისწყალ-თუთიის ელემენტი, ვერცხლი-თუთიის აკუმულატორი, ქრომ- თუთიის ელემენტი, ნიკელ-თუთიის აკუმულატორი, თუთია-ბრომის აკუმულატორი, თუთია-ქლორის აკუმულატორი და ა. შ. ძალიან მნიოშვნელოვანია თუთიის როლი თუთია-საჰაერო აკუმულატორებში, რომელიც უკანასკნელ წლებში ინტენსიურად მუშავდება თუთია-ჰაერის სისტემის საფუძველზე - აკუმულატორები კომპიუტერისათვის (ნოუთბუქები) და ამ სფეროში არის მნიშვნელოვანი წარმატება (უფრო მეტი მოცულობა და რესურსები, ვიდრე ლითიუმის ბატარეას, თვითღირებულება კი 3-ჯერ ნაკლები), ეს სისტემა ასევე პერსპექტიულია ძრავების გამშვებებისათვის (ტყვიის აკუმულატორი - 55ვტ×სთ/კგ, თუთია-ჰაერი - 220-300ვტ×სთ/კგ) და ელექტრომანქანებისათვის (გარბენი 900კმ). შედის მრავალი მაგარი სარჩილის შემადგენლობაში მათი ლღობის ტემპერატურის შემცირების გამო. თუთია ლატუნში არის მნიშვნელოვანი კომპონენტი. თუთიის ოქსიდი ფართოდ გამოიყენება მედიცინაში, როგორც ანტისეპტიკური და ანთებისსაწინააღმდეგო საშუალება. ასევე თუთიის ოქსიდი გამოიყენება საღებავების საწარმოებლად - თუთიის თეთრა.
თუთიის ქლორიდი - არის მნიშვნელოვანი ფლუსი მეტალების შედუღებისათვის და კომპონენტი ფიბრების წარმოებისათვის.
თუთიის ტელურიდი, სელენიდი, ფოსფიდი - ფართოდ გამოყენებადი ნახევარგამტარებია.
თუთიის სელენიდი გამოიყენება ოპტიკური მინების წარმოებისას ძალიან დაბალი შთანთქმის კოეფიციენტით საშუალო ინფრაწითელ დიაპაზონში, მაგალითად ნახშირმჟავას ლაზერებში.
.
თუთიის შემადგენლობა კვების პროდუქტებში
კვების პროდუქტებს შორის, რომელსაც ადამიანი საკვებად იყენებს თუთიის ყველაზე მაღალი შემცველობაა ხამანწკებში. თუმცა გოგრის თესლი შეიცავს მხოლოდ 26%-ით ნაკლებ თუთიას ვიდრე ხამანწკები. მაგალითად, 45გ ხამანწკების მიღებისას ადამიანი ღებულობს იმდენ თუთიას, რამდენსაც შეიცავს 60გ გოგრის თესლი. პრაქტიკულად თითქმის ყველა ხორბლეული შეიცავს თუთიას საკმაო რაოდენობით და ადვილად ათვისებადი ფორმით. ამიტომაც ბიოლოგიური მოთხოვნილება ადამიანის ორგანიზმისა თუთიაზე, ჩვეულებრივ მთლიანად უზრუნველყოფილია მარცვლეული პროდუქტების ყოველდღიური მოხმარებით (არარაფინირებული მარცვლეული).
ასევე, თუთიით მდიდარია ხორბალი და ხორბლის ქატო, ბატის ხორცი, ლობიო, ბარდა, სიმინდი, საქონლისა და ქათმის ხორცი, თევზი, საქონლის ღვიძლი, რძე.
მ ელემენტს შეიცავს ასევე ვაშლი, მსხალი, ქლიავი, ალუბალი, კარტოფილი, კომბოსტო, ჭარხალი და სტაფილო
თუთიის შემცველობა:
- ~ 0.25მგ/კგ - ვაშლი, ფორთოხალი, ლიმონი, ლეღვი, გრეიფუტი, ყველა ხორციანი ხილი, მწვანე ბოსტნეული, მინერალური წყალი.
- ~ 0.31მგ/კგ - თაფლი
- ~ 2 - 8მგ/კგ - ჟოლო, შავი მოცხარი, ფინიკი, ბოსტნეულის დიდი ნაწილი, ზღვის თევზის უმეტესობა, რძე, გასუფთავებული ბრინჯი, წარხალი ჩვეულებრივი და შაქრის, პომიდორი, კარტოფილი, პური, სატაცური, ნიახური, ბოლოკი.
- ~ 8 - 20მგ/კგ - ზოგიერთი მარცვლეული, საფუარი, ხახვი, ნიორი, ყავისფერი ბრინჯი, კვერცხი.
- ~ 20 - 50მგ/კგ - შვრიის და ქერის ფქვილი, კაკაო, ბადაგი, კვერცხის გული, კურდღლისა და წიწილის ხორცი, თხილი, ბარდა, ლობიო, მუხუდო, მწვანე ჩაი, გამხმარი საფუარი.
- ~ 30 - 85მგ/კგ - საქონლის ღვიძლი, ზოგიერთი თევზის სახეობა
- ~ 130 - 202მგ/კგ - გოგრის თესლი, მზესუმზირა.
ტოქსიკურობა
თუთიის იონები Zn2+ ტოქსიკურია. ხოლო მისი ყველა მარილი ტოქსიკურია ადამიანისათვის, განსაკუთრებით კი სულფატები და ქლორიდები. 1გრ თუთიის სულფატს ZnSO4 შეუძლია გამოიწვიოს მძიმე მოწამვლა. ქლორიდები, სულფატები და თუთიის ჟანგი შეიძლება წარმოიქმნას საკვები პროდუქტების თუთიის ან მოთუთიებულ ჭურჭლში შენახვისას. თუთიით მოწამვლისას ადგილი აქვს პანკრეასის ფიბროზულ გადაზრდას . თუთია აფერხებს ზრდას და ირღვევა ძვლების მინერალიზაციის პროცესი.
სისხლში თუთიის ჭარბ შემცველობას მივყავართ პროგრესირებად სისუსტემდე, მყესების რეფლექსების დაქვეითებას, სისხლიან დიარეას, კიდურების პარეზი. გახსნისას შეინიშნება ღვიძლის ნეკროზი და თეძოს ტავების დეკალციფიკაცია. თუთიის სულფატით ZnSO4 მოწამვლა იძლევა ანემიის ნათელ სურათს, ზრდის შეფერხებას, უშვილობას. თუთიის ჟანგით მოწამვლა ხდება მისი ორთქლის შესუნთქვით. ის ვლინდება პირის ღრუში ტკბილი გემოს შეგრძნებით, მადის დაქვეითებით ან სრული დაკარგვით, არც თუ ისე იშვიათად ძლიერ წყურვილს შეგრძნებით. წარმოიშობა დაღლილობა, შერყეული ჯანმრთელობის შეგრძნება, შევიწროება და ტკივილი გულმკერდის არეში. ხოლო 4-5 საათის შემდეგ ეს შეგრძნებები განვითარების მაქსიმუმს აღწევს. ეს პირველი პერიოდი იცვლება სიცივის შეგრძნებით ფეხებიდან, შემდეგ უცებ ციება, კანკალი 1-1.5 საათი და ტემპერატურა ადის 37.4°C-მდე, შემდეგ იწყება ძლიერი ოფლდენა. ავადმყოფი განიცდის მტვრევას მთელ სხეულში, ტკივილს კუნთებში, თავის ტკივილს, ხმაურს ყურებში, სიმშრალეს პირის ღრუსა და ყელში, გულისრევას, ზოგჯერ ღებინებას. იშვიათად - დიარეას. შარდში საქარი და ურობილინია. სისხლში შაქრის სემცველობა მნისვნელოვნად იზრდება.
ბიოლოგიური თვისებები

თუთიის შემცველი საკვები პროდუქტები
თუთია ორგანიზმის ნორმალური ფუნქციონირებისათვის აუცილებელი ელემენტია. თუთიის ნაერთთა ხსნარების პრეპარატები მედიცინაში გამოიყენება სადეზინფექციო საშუალებებად.
თუთია ფერმენტების შემადგენლობაში შედის, მონაწილეობს ჟანგვა-აღდგენით პროცესებში. ის ნერვული და შემაერთებელი ქსოვილის მნიშვნელოვანი კომპონენტია. დღე-ღამეში 10 მგ თუთია საკმარისია, რომ ბავშვის ორგანიზმი ადეკვატურად განვითარდეს.
თუთია დიდ როლს ასრულებს ორგანიზმის ჰორმონულ ფუნქციათა რეალიზებაში. თუთია ის მიკროელემენტია, რომელსაც შეიცავს ჰემოგლობინში შემავალი ჰემის ბიოსინთეზის გადამწყვეტ რეაქციაში მონაწილე ფერმენტი, აგრეთვე სუპეროქსიდდისმუტაზა - მნიშვნელოვანი ანტიოქსიდანტური ფერმენტი.. ის უშუალოდ ახდენს გავლენას ინსულინის პროდუქციასა და ფუნქციობაზე და ამით ინსულინდამოკიდებული პროცესების მთელ სპექტრზე.
თუთია შედის ასობით მეტალოფერმენტის აქტიური ცენტრის სტრუქტურულ შემადგენლობაში. ის აუცილებელია დნმ და რნმ-პოლიმერაზების ფუნქციობისთვის, რომლებიც ახორციელებენ მემკვიდრეობითი ინფორმაციის გადაცემას, ცილების ბიოსინთეზს (წარმოქმნას) და ორგანიზმის რეპარაციულ (განახლების) პროცესებს აკონტროლებენ.
მამაკაცებში თუთია მონაწილეობს ტესტოსტერონის (მამრობითი სასქესო ჰორმონის) სინთეზში და სასქესო ჯირკვლების ფუნქციობაში. სწორედ ამიტომ ორგანიზმში თუთიის დონესა და პოტენციას შორის მნიშვნელოვანი კავშირი არსებობს. თუთია აინჰიბირებს (ბოჭავს) 5-ალფა-რედუქტაზას, რითაც არეგულირებს ტესტოსტერონის მეტაბოლიტის დიჰიდროტესტოსტერონის დონეს (შეგახსენებთ: ამ უკანასკნელის სიჭარბე პროსტატის - წინამდებარე ჯირკვლის - ჰიპერპლაზიას განაპირობებს). თუთია აუცილებელია არა მხოლოდ მამაკაცის, არამედ ქალის ორგანიზმისთვისაც. მას შეიცავს ესტროგენებისთვის (მდედრობითი სასქესო ჰორმონებისთვის) განკუთვნილი რეცეპტორები (მგრძნობიარე წარმონაქმნები), რის გამოც თუთია ფაქტობრივად ესტროგენდამოკიდებული პროცესების რეგულატორად გვევლინება. თუთიას სასიცოცხლო მნიშვნელობა აქვს თიმუსის (მკერდუკანა ჯირკვალი) ფუნქციობისა და ორგანიზმის იმუნური სისტემის ნორმალური მდგომარეობისთვის. აღნიშნული მიკროელემენტი წარმოადგენს რეტინოლგადამტანი ცილის კომპონენტს, A და C ვიტამინებთან ერთად ასტიმულირებს ანტისხეულების სინთეზს და ავლენს ანტივირუსულ მოქმედებას, რითაც აფერხებს იმუნოდეფიციტის აღმოცენებას. თუთიას აქვს ჭრილობებისა და წყლულების შემხორცებელი მოქმედება, მონაწილეობს ყნოსვითი და გემოვნებითი აღქმის პროცესებში, აუცილებელია ცენტრალური ნერვული სისტემის ფუნქციობისთვის, მათ შორის - მეხსიერების პროცესებისთვისაც. თუთიას დიდი ოდენობით შეიცავს ხორბლის ქატო და ღივი, მზესუმზირისა და გოგრის თესლი (130-დან 202 მგ/კგ-მდე), საქონლის ღვიძლი, თევზის ზოგიერთი სახეობა (30-დან 85 მგ/კგ-მდე), ლობიო, ბარდა, მწვანე ჩაი, კურდღლისა და წიწილის ხორცი, ნიგოზი, კვერცხის გული, კაკაო (20-დან 50 მგ/კგ-მდე).
საინტერესო ფაქტები
გარდა ამისა, თუთია ითვლება სილამაზის ელემენტად. ძველ ჩინეთში (1500წ. ჩვ. წ.ა.) ქალები სახის კანს იზილავდნენ მარგალიტით, რომელიც ძალინ მდიდარია ამ მიკროელემენტით. ასეთი კოსმეტიკური პროცედურა სახის კანს აძლევდა ჯანსაღ შესახედაობას და განუმეორებელ ბრწყინვალებას. ეს გასაკვირი არ არის, რადგანაც თუთია აუმჯობესებს კანის ფერსა და გარეგნობას, აქტიურ მონაწილეობას ღებულობს ცხიმოვანი მჟავების დამუშავებაში და ამით გავლენას ახდენს რეგენერაციის პროცესზე. დაქუცმაცებული მარგალიტი გამოიყენებოდა კოსმეტიკაში პომადების, ჩრდილების და პუდრის დასამზადებლად. წარმოუდგენელია, მაგრამ ბევრი ჩინელი ქალი დღესაც ჭამენ მარგალიტის პუდრას ან იყენებენ კოცმეტიკას, რომელიც მის ექსრტაქტზეა დამზადებული.
მომხიბვლელობისა და ქალის სილამაზის ეტალონი დედოფალი კლეოპატრა თავის მომხიბვლელობას ინარჩუნებდა თხის რძის ვანების წყალობით რომელსაც ის ღებულობდა და რომელიც მდიდარია თუთიით.
ორგანიზმის დღიური ნორმა თუთიაზე ახალშობილებში არის 6მგ, რომელსაც ისინი იღებენ დედის რძიდან. ზრდასრული ადამიანისათვის აუცილებელია 15-20მგ, ორსული ქალებისათვის 30მგ. ყოველდღიურად ორგანიზმი ხარჯავს 3მგ ძვირფას მიკროელემნტს, თუთიას ოფლიანობის დროს.
ამერიკულმა საზოგადოებამ მეცნიერების პროგრესისათვის ერთ-ერთ კონფერენციაზე დაადგინა, რომ ”ვინაიდან თუთიის დეფიციტი ადამიანის ორგანიზმში ახდენს უარყოფით გავლენას მის ჯანმრთელობაზე, აფერხებს ზრდის პროცესს, ორგანიზმის განვითარებას და იწვევს მრავალ სხვა მტკივნეულ მდგომარეობას, თუთია უნდა იყოს აღიარებული, როგორც ორგანიზმის ნორმალური ფუნქციონირებისათვის აუცილებელი ელემენტი.” მოცემული ფაქტი რეზოლუციაში იქნა შეტანილი.
გეორგიევსკის დარბაზი - ერთ-ერთი ბრწყინვალე და გრანდიოზული დარბაზია მოსკოვის დიდ კრემლის სასახლეში, რომელსაც აქვს 18 დაგრეხილი (დახვეული) სვეტი, რომელიც ჩამოსხმულია თუთიისაგან (отлитых из цинка) და შემოსაზღვრულია ლამაზი ორნამენტებით, გამარჯვების ქანდაკებით დაფნის გვირგვინით, ასევე მოქანდაკე ი.პ. ვიტალის სამუშაოს სამოხსოვრო თარიღით. ერთ-ერთი ასეთი ქანდაკება შექმნილია უკრაინისა და რუსეთის გაერთიანების პატივსაცემად.
კარგად არის ცნობილი, რომ დიდი რაოდენობით თუთიაა შეიცავს გველის შხამი, განსაკუთრებით ჭრელი გველი და კობრა. ასევე ცნობილია, რომ თუთიის მარილები ახშობენ ამ შხამების აქტიურობას. ექსპერიმენტმა აჩვენა, რომ თუთიის მარილების ზემოქმედებით შხამი არ იშლება. ეს თითქოს ეწინააღმდეგება იმ მოსაზრებას, თუმცა მისი ახსნა შეიძლება. თუთიის მარალი შემცველობა შხამში - ეს არის საშუალება, რომლითაც გველი იცავს თავს საკუთარი შხამისაგან!
უამრავი გამოვლინებები თუთიის დეფიციტის დროს ორგანიზმში ხშირად მსგავსია იმისა რაც ვითარდება ნაადრევი დაბერების სინდრომის დროს.
თუთიის რაოდენობა მნიშვნელოვნად მცირდება პროდუქტების ზედმეტად გასუფღავებისა და გადამუსავების დროს. ამრიგად, ამრიგად, ყავისფერი ბრინჯი 6-ჯერ მეტ თუთიას შეიცავს ვიდრე გასუფთავებული თეთრი ბრინჯი.
იზოტოპები
ბუნებაში გვხვდება თუთია და მისი ხუთი სტაბილური იზოტოპი: 64Zn, 66Zn, 67Zn, 68Zn და 70Zn, რომელთაგან ყველაზე გავრცელებულია 64Zn (48.89%). ხელოვნურად შესაძლებელი გახდა მიეღოთ ცხრა რადიოაქტიური იზოტოპი. მათ შორის ყველაზე სიცოცხლისუნარიანია 65Zn, რომლის ნახევარდაშლის პერიოდია 245 დღე, მან გამოყენება ჰპოვა, როგორც იზოტოპურმა ინდიკატორმა.
მასალა მომზადებულია www.wikipedia.com -ის მიხედვით


